
将过量的CO2分别通入:①CaCl2溶液 ②Na2SiO3溶液 ③Ca(ClO)2溶液 ④饱和Na2CO3溶液 ⑤NaAlO2溶液。最终有沉淀生成的是
A.②④⑤ B.②③⑤ C.②⑤ D.①②③④⑤
科目:高中化学 来源: 题型:
对于100mL 1mol/L盐酸与锌粒的反应,采取下列措施能使反应速率加快的是
①升高温度;②改用100mL 3mol/L盐酸;③多用300mL 1mol/L盐酸;④用等量锌粉代替锌粒;⑤滴入少量CuSO4溶液
A.①②④⑤ B.①③④⑤ C.①②③④ D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列相关反应的离子方程式书写正确的是( )
A.4molFe 在5molCl2中点燃反应:5Cl2+4Fe=2FeCl2+2FeCl3
B.氯化铁溶液中通入硫化氢:2Fe3++H2S=2Fe2++S↓+2H+
C.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O
D.NaHCO3溶液中加入过量的Ba(OH)2溶液:
2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列氧化还原反应:2BrO3-+Cl2==Br2+2ClO3-,
5Cl2+I2+6H2O==2IO3-+10Cl-+12H+,
ClO3-+5Cl-+6H+==3Cl2↑+3H2O。
上述条件下,各微粒氧化性由强到弱的排列顺序正确的是
A.ClO3->BrO3->IO3->Cl2 B.BrO3->Cl2>ClO3->IO3-
C.BrO3->ClO3->Cl2>IO3- D.Cl2>BrO3->ClO3->IO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
有3份等质量的小苏打,第1份直接与过量盐酸反应;第2份先加热,使其部分分解后,再与过量盐酸反应;第3份先加热,使其完全分解后,再与过量盐酸反应。假若盐酸的物质的量浓度相同,实际消耗盐酸的体积分别为V1、V2和V3,则V1、V2和V3的大小关系正确的是
A.V1>V2>V3 B. V1>V3>V2 C. V2>V3>V1 D. V1=V2=V3
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组拟用50 mL NaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入的CO2气体过量生成NaHCO3,设计了如下实验步骤:
①用25 mL NaOH溶液吸收CO2气体,至CO2气体不再溶解;
②小火煮沸溶液1 min~2 min;
③在得到的溶液中加入另一半(25 mL)NaOH溶液,使其充分混合。此方案能制得较纯净的Na2CO3(第一步的实验装置如下图所示)
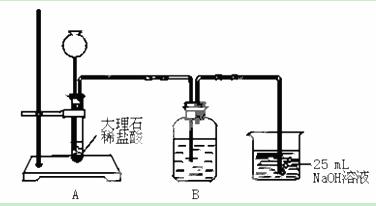
(1)写出①、③两步的化学反应的离子方程式① 。
③
(2)装置B中盛放的试剂是 ,作用是 。
(3)实验室中吸收尾气的方法很多。如下图装置中可以用吸收氨气的是 。
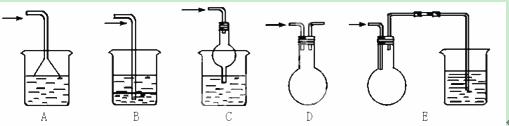
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学用语的表示正确的是
A.过氧化钠的电子式: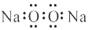 B.质子数为35、中子数为45的溴原子:
B.质子数为35、中子数为45的溴原子: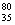 Br
Br
C.硫离子的结构示意图: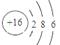 D.乙烯的结构简式:CH2CH2
D.乙烯的结构简式:CH2CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在A、B、C处分别充入等质量的X、H2、Y三种气体,当隔板静止时,A、C内的气体密度相等,下列说法正确的是
A.X的相对分子质量等于Y的相对分子质量
B.X的相对分子质量比Y的相对分子质量小
C.气体的体积:V(X)>V(H2)>V(Y)
D.物质的量:n(X)<n(H2)<n(Y)
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将20.0 g 14%的NaCl溶液跟30.0 g 24%的NaCl溶液混合,混合后 得到密度为1.17 g·cm-3的溶液。请计算:
得到密度为1.17 g·cm-3的溶液。请计算:
(1)混合后溶液中NaCl的质量分数为________。
(2)混合后溶液中NaCl的物质的量浓度为________。
(3)在1 000 g水中需加入________mol NaCl,才能使其浓度恰好与上述混合后溶液的浓度相等。(假设密度不变,计算结果保留1位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com