
【题目】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)![]() 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
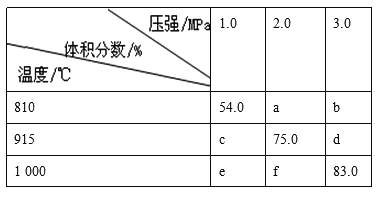
①b<f ②915℃、2.0 MPa时E的转化率为60% ③该反应是△S>0 ④K(1000℃)>K(810℃)
上述①~④中正确的有( )
A. 4个 B. 3个 C. 2个 D. 1个
【答案】A
【解析】①a和b是温度相同,压强不同,F为固体,增大压强,平衡向逆反应方向移动,即a>b,c>75%>54.0%,同压强下,升高温度,G的体积分数增大,说明升高温度,平衡向正反应方向进行,此反应的正反应方向是吸热反应,因此G的体积分数中a<75%<f,从而得出b<f,故①正确;②令E为1mol,转化率为a,则有2a/(1+a)×100%=75%,即a为60%,故②正确;③F为固体,E和G为气体,且G的系数大于E,此反应是熵增,即△S>0,故③正确;④K只受温度的影响,此反应是吸热反应,升高温度,平衡向正反应方向进行,即K(1000℃)>K(800℃),故④正确;综上所述,选项A正确。


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 95℃时纯水的pH<7,说明加热可导致水呈酸性
B. 将pH=3的CH3COOH溶液加水稀释10倍后pH=4
C. 0.2mol/L的盐酸1L加水到2L后,溶液的pH=1
D. NaHCO3 溶液水解反应的方程式:HCO3-+H2O![]() H3O++CO32--
H3O++CO32--
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )
A. c(NH4+)相等的(NH4)2SO4溶液、NH4HSO4和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2 (SO4)]<c(NH4HSO4)<c(NH4Cl)
B. 欲除去CuCl2溶液中混有少量的FeCl3,可加入CuO
C. 0.2mol/LHCl溶液与等体积0.05 mol/L Ba(OH)2溶液混合后,溶液的pH=1
D. 0.2mol/L的NaHCO3溶液中:c(H+) + c(H2CO3)=c(CO32-) + c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有镁铝合金共3.90克,与500ml 2.00mol/L盐酸(足量)反应,生成的气体在标准状况下体积为4.48L,若反应后所得溶液的体积稀释为1000ml,求:
(1)求镁铝合金中铝的物质的量。
(2)求镁铝合金中镁的质量分数。
(3)求反应后溶液中Cl-的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水的综合利用可以制备金属钠和镁,其流程如下图所示:

下列说法不正确的是( )
A. 要检验母液中是否含氯离子应当用硝酸酸化的硝酸银溶液进行实验
B. 上述流程MgCl2制取Mg的反应中,MgCl2既是氧化剂又是还原剂
C. 上述流程中的变化都属于化学变化
D. 上述流程中生成Mg(OH)2沉淀的离子方程式为:Mg:2++Ca(OH)2=Mg(OH)2+Ca2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用氟碳铈矿(主要成分CeCO3F)提取CeCl3的一种工艺流程如下:

请回答下列问题:
(1)已知CeCO3F中C为+4价,Ce元素的化合价为_______。焙烧后Ce元素被________。(填“氧化”或“还原”)
(2)酸浸过程中用稀硫酸和H2O2替换HCl不会造成环境污染。写出稀硫酸、H2O2与CeO2反应的离子方程式:_______________________________。
(3)向Ce(BF4)3中加入KCl溶液的目的是__________________。
(4)CeCl3 .6H2O属于___________物(填“纯净”或“混合物”)
(5)准确称取0.75gCeCl3样品置于锥形瓶中,加入适量过硫酸铵溶液将Ce3+氧化为Ce4+,然后加入25ml 0.10mol/l (NH4)2Fe(SO4)2与之恰好反应完。(已知:Fe2++Ce4+=Ce3++Fe3+)该样品中CeCl3的质量分数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下,在27.5g 水中溶解12.5gCuSO4· 5H2O,溶液恰好达到饱和,该溶液的密度为2.0g/cm3。求:
①该溶液中CuSO4的物质的量浓度为____________。
②取出10.0 mL该溶液,配成物质的量浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是____mL。
(2)有一瓶子,盛满氢气时总质量为m1g,盛满氧气时总质量为m2g。若改装入二氧化碳气体,该瓶总质量为__________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据下列图示,写出反应的热化学方程式。

A.___________________________________。
B.___________________________________。
(2)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式为___________________。
(3)如图是598 K时,N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为_______________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com