
科目:高中化学 来源: 题型:
镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成.为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
已知:①NiCl2易溶水,Fe3+不能氧化Ni2+
②该温度下一些难溶物的Ksp及沉淀析出的理论pH如下表所示:
| Ksp | 开始沉淀pH | 沉淀完全pH |
| |
| Al(OH)3 | 1.9×10-33 | 3.43 | 4.19 | |
| Fe(OH)3 | 3.8×10-38 | 2.53 | 2.94 | |
| Ni(OH)2 | 1.6×10-14 | 7.60 | 9.75 | |
| NiC2O4 | 4.0×10-10 | —— | —— |
回答下列问题:
(1)该工艺流程中多次重复利用的一种实验基本操作是 。
(2)步骤①所留残渣的主要成分为 (填物质名称)
(3)根据上表数据判断步骤②依次析出沉淀Ⅱ______和沉淀Ⅲ______(填化学式),
控制两种沉淀析出可利用 。
A.pH试纸 B.石蕊指示剂 C.pH计
(4)已知实验温度时的溶解度:NiC2O4>NiC2O4•H2O>NiC2O4•2H2O,则步骤③的化学反应方程式是 。
(5)C可被E氧化,写出步骤④的离子反应方程式 。
(6)FeCl3和AlCl3 的混合溶液中加入NaOH溶液,若Fe(OH)3和Al(OH)3同时存在,则c(Fe3+)/c(Al3+)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物的天然提取和人工合成往往得到的是混合物,假设给你一种这样的有机混合物让你研究,一般要采取的几个步骤是
A.分离、提纯→确定化学式→确定实验式→确定结构式
B.分离、提纯→确定实验式→确定化学式→确定结构式
C.分离、提纯→确定结构式→确定实验式→确定化学式
D.确定化学式→确定实验式→确定结构式→分离、提纯
查看答案和解析>>
科目:高中化学 来源: 题型:
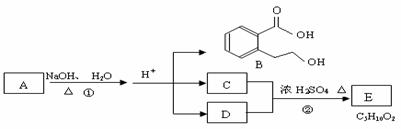 下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应;C和D的相对分子质量相等,且E为无支链的化合物。根据下图回答问题:
下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应;C和D的相对分子质量相等,且E为无支链的化合物。根据下图回答问题:
(1)C分子中的官能团名称是 ______________;化合物B不能发生的反应是 (填字母序号):
a 加成反应 b取代反应 c消去反应 d酯化反应 e水解反应 f 置换反应
(2)反应②的化学方程式是_____ _。
(3)反应②实验中加热的目的是(从速率和平衡两个角度分析)
(4) A的结构简式是 __________________ 。
(5)同时符合下列三个条件的B的同分异构体的数目有 个。
I.含有间二取代苯环结构 Ⅱ.属于非芳香酸酯 Ⅲ.与 FeCl3 溶液发生显色反应。
写出其中任意一个同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
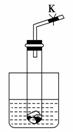 设计学生实验要注意安全、无污染、现象明显。根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(如图)。若关闭K,不能使反应停止,可将试管从烧杯中取出(会有部分气体逸出)。下列气体的制取宜使用该装置的是( )
设计学生实验要注意安全、无污染、现象明显。根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(如图)。若关闭K,不能使反应停止,可将试管从烧杯中取出(会有部分气体逸出)。下列气体的制取宜使用该装置的是( )
A.用二氧化锰(粉末)与双氧水制氧气 B.用锌粒与稀硫酸制氢气
C.用硫化亚铁(块状)与盐酸制硫化氢 D.用碳酸钙(块状)与稀硫酸制二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
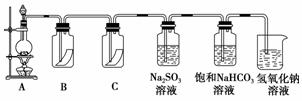
“84消毒液”与硫酸溶液反应可以制取氯气(NaClO+NaCl+H2SO4===Na2SO4+Cl2↑+H2O)。为探究氯气的性质,某同学利用此原理制氯气并设计了如下所示的实验装置。
请回答下列问题:
(1)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是________________________,请提出合理的改进方法________________________________________________________________________。
(2)为了验证氯气的氧化性,将氯气通入Na2SO3溶液中,写出氯气与Na2SO3溶液反应的离子方程式___________________________________________________________
________________________________________________________________________。
(3)氯气通入饱和NaHCO3溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验证明氯气与水反应的生成物中含有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒沙特列原理来解释的是
A.加压有利于SO2与O2反应生成SO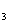
B.密闭容器中发生反应H2(g)+I2(g) 2HI(g),增大压强时容器中颜色加深。
2HI(g),增大压强时容器中颜色加深。
C.将混合气中的氨气液化后不停的分离出来,有利于合成氨的反应
D.用过量氮气与氢气反应可以提高氢气的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
①常温下,0.1 mol·L-1某一元酸(HA)溶液中 =1×10-8,由水电离出的c(H+)=1×10-11 mol·L-1
=1×10-8,由水电离出的c(H+)=1×10-11 mol·L-1
②浓度为0.1mol·L-1的某酸式盐NaHA溶液中c(Na+) =c(A2-)+c(HA-) +c(H2A)
③pH=12的氨水与pH=2的盐酸等体积混合c(NH4+)>c(Cl-)>c(OH-)>c(H+)
④浓度均为0.1mol·L-1的小苏打溶液与烧碱溶液等体积混合
c(Na+)+c(H+)=2c(CO32-)+c(OH-)
A.①②③ B.①②④ C.①③④ D.全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com