
| A£® | £Ø1£©£Ø2£©£Ø3£©£Ø4£© | B£® | £Ø2£©£Ø3£©£Ø4£© | C£® | £Ø3£©£Ø4£© | D£® | £Ø3£© |
·ÖĪö Ķ¬ĪĀĶ¬Ń¹ĻĀµČĢå»żµÄCO2ŗĶSO2Į½ÖÖĘųĢåµÄĪļÖŹµÄĮæĻąµČ£®
£Ø1£©øł¾Żm=nMÅŠ¶Ļ£»
£Ø2£©Ķ¬ĪĀĶ¬Ń¹ĻĀĘųĢåµÄĆܶČÖ®±ČµČÓŚĘäĦ¶ūÖŹĮæÖ®±Č£»
£Ø3£©·Ö×ÓŹżÄæÖ®±ČµČÓŚĘäĪļÖŹµÄĮæÖ®±Č£»
£Ø4£©CO2ŗĶSO2·Ö×Óŗ¬ÓŠµē×ÓŹż·Ö±šĪŖ22”¢32£®
½ā“š ½ā£ŗĶ¬ĪĀĶ¬Ń¹ĻĀµČĢå»żµÄCO2ŗĶSO2Į½ÖÖĘųĢåµÄĪļÖŹµÄĮæĻąµČ£®
£Ø1£©CO2ŗĶSO2µÄĦ¶ūÖŹĮæ²»ĻąµČ£¬øł¾Żm=nMæÉÖŖ£¬¶žÕßÖŹĮæ²»ĻąµČ£¬¹Ź“ķĪó£»
£Ø2£©Ķ¬ĪĀĶ¬Ń¹ĻĀĘųĢåµÄĆܶČÖ®±ČµČÓŚĘäĦ¶ūÖŹĮæÖ®±Č£¬CO2ŗĶSO2µÄĦ¶ūÖŹĮæ²»ĻąµČ£¬Ōņ¶žÕßĆÜ¶Č²»ĻąµČ£¬¹Ź“ķĪó£»
£Ø3£©øł¾ŻN=nNAæÉÖŖ£¬·Ö×ÓŹżÄæÖ®±ČµČÓŚĘäĪļÖŹµÄĮæÖ®±Č£¬Ōņ¶žÕßĖłŗ¬·Ö×ÓŹżÄæĻąµČ£¬¹ŹÕżČ·£»
£Ø4£©CO2ŗĶSO2·Ö×Óŗ¬ÓŠµē×ÓŹż·Ö±šĪŖ22”¢32£¬¶žÕßŗ¬ÓŠµē×ÓŹż²»ĻąµČ£¬¹Ź“ķĪó£¬
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄĮæÓŠ¹Ų¼ĘĖć”¢°¢·üŁ¤µĀĀŽ¶ØĀɼ°ĘäĶĘĀŪ£¬×¢Ņāøł¾ŻPV=nRTĄķ½ā°¢·üŁ¤µĀĀŽ¶ØĀɼ°ĘäĶĘĀŪ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģś·ŪÓėŃĪĖį·“Ó¦£ŗ2Fe+2HØT2Fe3++H2”ü | |
| B£® | ŃĪĖįÓėCaCO3·“Ó¦£ŗCaCO3+2HØTCa2++H2O+CO2”ü | |
| C£® | ¶žŃõ»ÆĢ¼ÓėĖ®·“Ó¦£ŗCO2+H2ØTCO32-+2H+ | |
| D£® | ŃĪĖįÓėĒāŃõ»ÆĶČÜŅŗ·“Ó¦£ŗH++OHØTH2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ÓŠA”¢D”¢E”¢G”¢M”¢LĮłÖÖĒ°ĖÄÖÜĘŚµÄŌŖĖŲ£®AŌŖĖŲµÄµ„ÖŹ£¬ŹĒ×īĒįµÄĘųĢ壬DŌ×ÓŗĖĶāµē×ÓÓŠ11ŌĖ¶ÆדĢ¬£¬EµÄøŗŅ»¼ŪĄė×ÓµÄŗĖĶā3p¹ģµĄČ«³äĀś£®GŌ×ÓµÄ2p¹ģµĄÓŠ2øöĪ“³É¶Ōµē×Ó£¬¶ĢÖÜĘŚŌŖĖŲMŌ×ÓÓėGŌ×Ó¾ßÓŠĻąĶ¬µÄ¼Ū²ćµē×ÓÅŲ¼£®LĪ»ÓŚÖÜĘŚ±ķµŚ12ׯŠŠĒŅŹĒĮłÖÖŌŖĖŲÖŠŌ×ÓŠņŹż×ī“óµÄ£®ĻĀĶ¼ŹĒÓÉM”¢LŠĪ³ÉµÄ»ÆŗĻĪļR£¬Ę侧°ū½į¹¹ČēĶ¼ĖłŹ¾£®
ÓŠA”¢D”¢E”¢G”¢M”¢LĮłÖÖĒ°ĖÄÖÜĘŚµÄŌŖĖŲ£®AŌŖĖŲµÄµ„ÖŹ£¬ŹĒ×īĒįµÄĘųĢ壬DŌ×ÓŗĖĶāµē×ÓÓŠ11ŌĖ¶ÆדĢ¬£¬EµÄøŗŅ»¼ŪĄė×ÓµÄŗĖĶā3p¹ģµĄČ«³äĀś£®GŌ×ÓµÄ2p¹ģµĄÓŠ2øöĪ“³É¶Ōµē×Ó£¬¶ĢÖÜĘŚŌŖĖŲMŌ×ÓÓėGŌ×Ó¾ßÓŠĻąĶ¬µÄ¼Ū²ćµē×ÓÅŲ¼£®LĪ»ÓŚÖÜĘŚ±ķµŚ12ׯŠŠĒŅŹĒĮłÖÖŌŖĖŲÖŠŌ×ÓŠņŹż×ī“óµÄ£®ĻĀĶ¼ŹĒÓÉM”¢LŠĪ³ÉµÄ»ÆŗĻĪļR£¬Ę侧°ū½į¹¹ČēĶ¼ĖłŹ¾£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
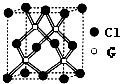 A”¢B”¢C”¢D”¢E”¢F”¢GĪŖŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĒ°ĖÄÖÜĘŚŌŖĖŲ£®A”¢FŌ×ÓµÄ×īĶā²ćµē×ÓŹż¾łµČÓŚĘäÖÜĘŚŠņŹż£®FŌ×ӵĵē×Ó²ćŹżŹĒAµÄ3±¶£» BŌ×ÓŗĖĶāµē×Ó·Ö“¦3øö²»Ķ¬Äܼ¶£®ĒŅĆæøöÄܼ¶ÉĻÅŲ¼µÄµē×ÓŹżĻąĶ¬£»AÓėCŠĪ³ÉµÄ×ī¼ņµ„·Ö×ÓĪŖČż½Ē׶ŠĪ£»DŌ×Óp¹ģµĄÉĻ³É¶Ōµē×ÓŹżµČÓŚĪ“³É¶Ōµē×ÓŹż£»EŌ×ÓŗĖĶāĆæøöŌ×Ó¹ģµĄÉĻµÄµē×Ó¶¼ŅŃ³É¶Ō£®EÓėFĶ¬ÖÜĘŚ£»GµÄŌ×ÓŠņŹżµČÓŚA”¢C”¢D”¢F ĖÄÖÖŌŖĖŲŌ×ÓŠņŹżÖ®ŗĶ£®
A”¢B”¢C”¢D”¢E”¢F”¢GĪŖŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĒ°ĖÄÖÜĘŚŌŖĖŲ£®A”¢FŌ×ÓµÄ×īĶā²ćµē×ÓŹż¾łµČÓŚĘäÖÜĘŚŠņŹż£®FŌ×ӵĵē×Ó²ćŹżŹĒAµÄ3±¶£» BŌ×ÓŗĖĶāµē×Ó·Ö“¦3øö²»Ķ¬Äܼ¶£®ĒŅĆæøöÄܼ¶ÉĻÅŲ¼µÄµē×ÓŹżĻąĶ¬£»AÓėCŠĪ³ÉµÄ×ī¼ņµ„·Ö×ÓĪŖČż½Ē׶ŠĪ£»DŌ×Óp¹ģµĄÉĻ³É¶Ōµē×ÓŹżµČÓŚĪ“³É¶Ōµē×ÓŹż£»EŌ×ÓŗĖĶāĆæøöŌ×Ó¹ģµĄÉĻµÄµē×Ó¶¼ŅŃ³É¶Ō£®EÓėFĶ¬ÖÜĘŚ£»GµÄŌ×ÓŠņŹżµČÓŚA”¢C”¢D”¢F ĖÄÖÖŌŖĖŲŌ×ÓŠņŹżÖ®ŗĶ£® £»»Ų“šEÓėFŌ×ӵĵŚŅ»µēĄėÄܵē󊔹ŲĻµŌõŃł£¬ŌŅņŹĒMgŌ×Ó3sÄܼ¶ĪŖČ«ĀśĪČ¶Ø½į¹¹£¬ÄÜĮæ½ĻµĶ£»
£»»Ų“šEÓėFŌ×ӵĵŚŅ»µēĄėÄܵē󊔹ŲĻµŌõŃł£¬ŌŅņŹĒMgŌ×Ó3sÄܼ¶ĪŖČ«ĀśĪČ¶Ø½į¹¹£¬ÄÜĮæ½ĻµĶ£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | FeO²»ĪČ¶Ø£¬ŌŚæÕĘųÖŠ¼ÓČČŃøĖŁ±»Ńõ»Æ³ÉFe2O3 | |
| B£® | 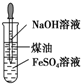 ÓÉĶ¼Ź¾²Ł×÷æÉÖĘČ”Fe£ØOH£©2 | |
| C£® | Fe3O4”¢Fe£ØOH£©3¶¼æÉŅŌÓÉ»ÆŗĻ·“Ó¦ÖĘµĆ | |
| D£® | Fe£ØOH£©3½ŗĢå³ŹŗģŗÖÉ«”¢ĶøĆ÷£¬ÄÜ·¢Éś¶”“ļ¶ūĻÖĻó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe2O3æÉŅŌ×öÓĶĘįµÄŃÕĮĻ | B£® | Al2O3æÉÓĆ×÷ÄĶ»š²ÄĮĻ | ||
| C£® | ĶõĖ®æÉŅŌµńæĢ²£Į§ | D£® | ³ąĢśæóæÉÓĆ×÷Į¶ĢśµÄŌĮĻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ÓĆ²¬×÷“߻ƼĮ | B£® | ½µµĶĪĀ¶Č | ||
| C£® | ĖõŠ”Ģå»żŌö“óŃ¹Ēæ | D£® | Ōö“ó½Ó“„Ć껿 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 150mL 1mol•L-1 ĀČ»ÆÄĘČÜŅŗ | B£® | 75mL 1mol•L-1 ĀČ»ÆøĘČÜŅŗ | ||
| C£® | 150mL 3mol•L-1 ĀČ»Æ¼ŲČÜŅŗ | D£® | 75mL 2mol•L-1 ĀČ»Æ±µČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
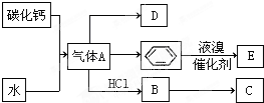
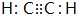 £»DµÄæռ乹ŠĶĪŖĘ½Ćę½į¹¹£¬¼ü½ĒĪŖ120”ć£»
£»DµÄæռ乹ŠĶĪŖĘ½Ćę½į¹¹£¬¼ü½ĒĪŖ120”ć£» +Br2 $\stackrel{FeBr_{3}}{”ś}$
+Br2 $\stackrel{FeBr_{3}}{”ś}$ +HBr£¬Ęä·“Ó¦ĄąŠĶĪŖČ”“ś·“Ó¦£®
+HBr£¬Ęä·“Ó¦ĄąŠĶĪŖČ”“ś·“Ó¦£®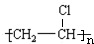 £¬Ęä·“Ó¦ĄąŠĶĪŖ¼Ó¾Ū·“Ó¦£®
£¬Ęä·“Ó¦ĄąŠĶĪŖ¼Ó¾Ū·“Ó¦£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com