
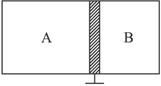
A.pA变小、pB变大 B.pA变小、pB不变
C.pA不变、pB不变 D.pA变小、pB变小
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:阅读理解
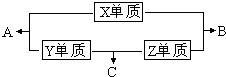 X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
| ||
| △ |
| ||
| △ |
| 加热 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源:高中化学习题 题型:021
如下图所示的密闭筒形容器内,有一活塞位于距一端的全长1/4处,在标准状况下若将![]() 混合气点燃引爆,活塞先左弹,后右滑,恢复原温度后,活塞停留在筒形容器的中央,则原
混合气点燃引爆,活塞先左弹,后右滑,恢复原温度后,活塞停留在筒形容器的中央,则原![]() 的体积比是下列中的
的体积比是下列中的

[ ]
A.![]()
B.![]()
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源:高中化学习题1 题型:021
如下图所示的密闭筒形容器内,有一活塞位于距一端的全长1/4处,在标准状况下若将![]() 混合气点燃引爆,活塞先左弹,后右滑,恢复原温度后,活塞停留在筒形容器的中央,则原
混合气点燃引爆,活塞先左弹,后右滑,恢复原温度后,活塞停留在筒形容器的中央,则原![]() 的体积比是下列中的
的体积比是下列中的

[ ]
A.![]() B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省潍坊市高三3月第一次模拟考试化学试卷(解析版) 题型:选择题
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对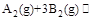
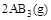 化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
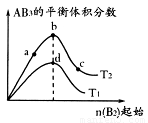
A.在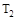 和
和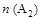 不变时达到平衡,
不变时达到平衡,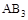 的物质的量大小为:c>b>a
的物质的量大小为:c>b>a
B.若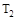 >
>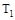 ,则正反应一定是放热反应
,则正反应一定是放热反应
C.达到平衡时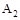 的转化率大小为:b>a>c
的转化率大小为:b>a>c
D.若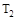 >
>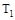 ,达到平衡时b、d点的反应速率为
,达到平衡时b、d点的反应速率为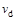 >
>
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com