
下列关于物质性质变化的比较,不正确的是
A.酸性强弱:HIO4>HBrO4>HClO4 B.原子半径大小:Na>S>O
C.碱性强弱:KOH>NaOH>LiOH D.金属性强弱: Na>Mg>Al
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源:2015-2016学年湖北省高二下学期期中考试化学试卷(解析版) 题型:选择题
下列离子晶体晶格能比较正确的是( )
A.KCl>NaCl>BaO>CaO B.NaCl>KCl>CaO>BaO
C.CaO>BaO>NaCl>KCl D.CaO>BaO>KCl>NaCl
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三第二轮训练五化学试卷(解析版) 题型:选择题
有关煤的综合利用如图所示.下列说法正确的是( )
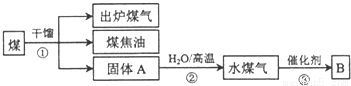
A.煤和水煤气均是二次能源
B.煤中含有苯、甲苯、二甲苯等有机物
C.①是将煤在空气中加强热使其分解的过程
D.B为甲醇或乙酸时,原子利用率均达到100%
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东汕头金山中学高二下第十二周练化学卷(解析版) 题型:选择题
三氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是
A.氯化硼液态时能导电而固态时不导电
B.硼原子以sp3杂化
C.氯化硼遇水蒸气会产生白雾
D.氯化硼分子属极性分子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:填空题
氢氧燃料电池是符合绿色化学理念的新型电池。电池装置如图所示,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

请回答下列问题:
(1)氢氧燃料电池的能量转化主要形式是________,在导线中电子流动方向为________(用a、b表示)。
(2)负极反应式为__________________________________________________________。
(3)电极表面镀铂粉的原因是_____________________________________________。
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断地提供电能。因此大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2 2LiH
2LiH
Ⅱ.LiH+H2O===LiOH+H2↑
①反应Ⅰ中的还原剂是____________,反应Ⅱ中的氧化剂是____________。
②已知LiH固体密度为0.82 g/cm3。用锂吸收224 L(标准状况)H2,生成的LiH体积与被吸收的H2体积之比为________。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为________ mol。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:选择题
有A、B、C、D、E五种短周期的主族元素,其原子序数依次增大。其中只有C是金属,D的单质是黄色固体,A、B、D在周期表中的相对位置关系如图所示,下列说法正确的是
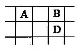
A.E元素位于周期表中的第三周期、ⅥA族
B.B的简单阴离子比D的简单阴离子还原性强
C.B与C形成的化合物中一定含有共价键
D.A、B两元素形成的常见化合物的分子中均含有极性键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:选择题
下列各组物质所含化学键类型完全相同的是
A.HNO3和NH4NO3 B.NaOH和KCl C.NaN3和CaO2 D.AlCl3和MgCl2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高二下期中理科化学试卷(解析版) 题型:选择题
鉴定1,3-二氯丙烷中氯元素的存在,下列描述正确的是
A.加入NaOH的溶液,加热,冷却后加入AgNO3溶液
B.加入NaOH溶液,加热,冷却后加入足量稀硝酸酸化,再加入AgNO3溶液
C.在氯乙烷中直接加入AgNO3溶液
D.加蒸馏水,充分搅拌后,加入AgNO3溶液
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:实验题
硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如图:
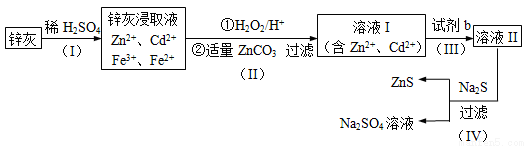
(1)为提高锌灰的浸取效率,不采用的方法是______________(填序号)
①研磨 ②搅拌 ③多次浸取 ④升高温度 ⑤加压
(2)步骤Ⅱ所得滤渣中的物质是______________(写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为______________。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是______________;
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取.化学反应方程式为______________。
③已知Na2SO4•10H2O及Na2SO4的溶解度随温度变化曲线如图。从滤液中得到Na2SO4•10H2O的操作方法是______________。
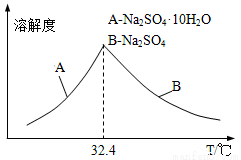
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液.则理论上所用锌灰中含有锌元素的质量为______________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com