
【题目】在一定温度下,将气体X和气体Y 各0.16 mol充入10 L 恒容密闭容器中,发生反应:X(g)+ Y(g)![]() 2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表。下列说法正确的是 ( )
2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表。下列说法正确的是 ( )
t / min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. 反应前2min的平均速率v(Z)=2.0×10-5 mol/(L·min)
B. 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C. 该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2 mol Z,平衡时X的物质的量浓度减小
【答案】C
【解析】A、根据v=△c/t计算出Y的速率为(0.160.12)/(10×2)mol/(Lmin)=0.002mol/(Lmin),根据速率之比等于化学计量数之比可得Z的速率为2×0.002mol/(Lmin)=0.004mol/(Lmin),A错误;B、由于该反应为放热反应,降低温度时,平衡正向移动,反应达到新平衡前v(逆)<v(正),B错误;C、根据方程式可知
X(g)+Y(g)![]() 2Z(g)
2Z(g)
起始浓度(mol/L) 0.016 0.016 0
转化浓度(mol/L) 0.006 0.006 0.012
平衡浓度(mol/L) 0.01 0.01 0.012
所以平衡常数K=0.0122/(0.01×0.01)=1.44,C正确;D、假设将0.2molZ在另一容器中建立与原平衡成等效平衡的体系,再将该体系加入到原容器中,由于该反应前后气体体积不变,所以压强对平衡的移动没有影响,所以加入后,X的体积分数不变,但X的物质的量增加,浓度增大,D错误;答案选C。


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】电解CuSO4溶液时,若要达到如下三个要求:①阳极质量减小;②阴极质量增加;③电解质溶液中Cu2+浓度不变。则选用的电极是( )
A.纯铜作阳极,含锌、银的铜合金作阴极
B.铁作阳极,铜作阴极
C.石墨作阳极,铂作阴极
D.含锌、银的铜合金作阳极,纯铜作阴极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. Na2O2分子中所有原子最外层均达到8电子稳定结构
B. NH4Cl、MgCl2均为离子化合物,均含有离子键和共价键
C. 同周期第ⅠA族元素和第ⅦA族元素之间只能形成离子化合物
D. NH4Cl仅由非金属元素组成,所以它是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于工农业生产和日常生活中与化学有关的问题,下列认识不正确的是
A.含有氯化钠融雪剂的使用会加快桥梁的腐蚀
B.铝合金的大量使用是因为人们能用焦炭等还原剂从氧化铝中获取铝
C.光缆在信息产业中有广泛应用,制造光缆的主要材料是二氧化硅
D.高温结构陶瓷氮化硅(Si3N4)具有较高的硬度和耐磨性,可用于制造汽车发动机
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①甲醛(HCHO)与葡萄糖化学性质相似,都具有还原性。②甲酸钙易溶于水。为探究过量甲醛和新制Cu(OH)2反应的产物,进行如下实验。
(1)在右图装置中进行实验,向a中加入0.5 mol·L-1CuSO4溶液50 mL和5 mol·L-1NaOH溶液100 mL,振荡,再加入40%的甲醛溶液50 mL,缓慢加热20分钟后冷却至室温。
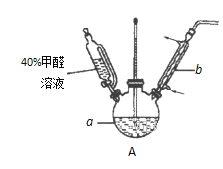
①仪器a的名称是_____________;
②能说明甲醛具有还原性的实验现象是______________。
(2)上述实验有副反应发生,产生的气体为CO、H2中的一种或两种。为确认气体成分,将装置A和如下图所示装置连接后进行实验。
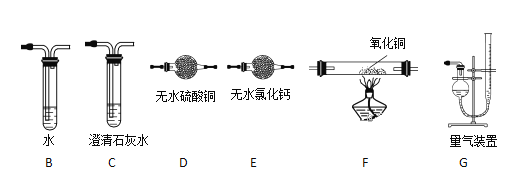
依次连接的合理顺序为A→B→___→____→____→____→G,装置B的作用是_________。有H2的实验现象是_________________________。
(3)已知HCHO![]() HCOOH
HCOOH![]() H2CO3。设计实验证明a中甲醛中的碳元素未被氧化成+4价。写出实验操作、现象、结论______________________。
H2CO3。设计实验证明a中甲醛中的碳元素未被氧化成+4价。写出实验操作、现象、结论______________________。
(4)反应后a中有红色固体产生,为探究其组成,提出如下假设:
假设一:只有Cu2O。 假设二:只有Cu。
假设三:Cu2O和CuO 假设四:________________________ ;
假设_______明显不成立,理由是___________________________ 。
进行如下实验(以下每步均充分反应):

已知:Cu2O ![]() [Cu(NH3)4]+(无色)
[Cu(NH3)4]+(无色)![]() [Cu(NH3)4]2+(蓝色)
[Cu(NH3)4]2+(蓝色)
①锥形瓶ii中固体完全溶解得深蓝色溶液的离子方程式为____________________;
②将容量瓶ii中的溶液稀释100倍后,溶液的颜色与容量瓶i相近。由此可知固体产物的组成及物质的量之比约为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在可逆反应:2A(g)+3B(g)![]() xC(g)+D(g)中,已知:起始浓度A为5mol/L,B为3mol/L,C的反应速率为0.5mol/(L·min),2min后,测得D的浓度为0.5mol/L。则关于此反应的下列说法正确的是( )
xC(g)+D(g)中,已知:起始浓度A为5mol/L,B为3mol/L,C的反应速率为0.5mol/(L·min),2min后,测得D的浓度为0.5mol/L。则关于此反应的下列说法正确的是( )
A. 2min末时A和B的浓度之比为5:3
B. x=1
C. 2min末时B的浓度为1.5mol/L
D. 2min末时A的消耗浓度为0.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将10.0g碳酸钙放入一定量稀盐酸中恰好完全反应,试计算:
(1)生成标准状况下的二氧化碳气体多少升?(不考虑CO2在水中的溶解)
(2)所得溶液中氯化钙的物质的量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学无处不在,下列与化学有关的说法不正确的是
A.侯氏制碱法的工艺过程中应用了物质溶解度的差异
B.碘是人体必需微量元素,国家规定食盐必须加碘。故炒菜时应在菜快出锅时放盐比较好
C.单质硅常用做光导纤维的材料,这与硅的半导体性能有一定关系
D.高压钠灯发出的黄光射程远、透雾能力强,常用做路灯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com