
下列分子或离子在指定条件的分散系中能大量共存的是
A. Ca(NO3) 2溶液中: Fe2+、H+、Cl—、SO42—;
B.使pH试纸变蓝的溶液中:K+、NH4+、S-、SO32-;
C.水电离出的c(H+)=10-12 mol·L-1的溶液中:Na+、Ba2+、HCO3—、CH3COO-[;
D.透明的强酸性溶液中: Al3+、Fe3+、Cl-、SO42
科目:高中化学 来源: 题型:
下列的操作方法正确的是
A.用蒸发的方法除去食盐水中的泥沙
B.用蒸馏的方法将自来水制成蒸馏水
C.分液漏斗下层的液体从下面放出,上层的液体应换一个烧杯接收
D.将22.4L氯化氢溶于水中,配成1L的溶液,即得1mol/L的盐酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是( )
A.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2
B.海水蒸发制海盐的过程中只发生了化学变化
C.海水中含有镁元素,只需经过物理变化就可以得到镁单质
D.目前工业上直接由海水提取I2
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图所示,A为银白色金属,A、B、C、D、E、F中均含有同一种元素。常温下G为液态,H为气态。
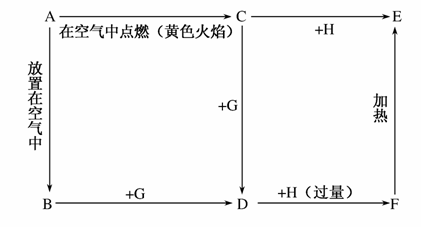
试回答:
(1)写出化学式:C________,D________,F________,H________。
(2)A与水反应的离子方程式为__________________ __________________________。
(3)写出F→E的化学方程式:____________________ _______________________。
(4)若向E的饱和溶液中通入足量的H,实验现象为______________________。
(5)写出F的一种用途______________________ __________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
不能用于判断金属失电子能力强弱的是
A.同主族金属元素原子半径大小
B.1 mol金属单质在反应中失去电子的多少
C.水溶液中金属间发生的置换反应
D.金属元素最高价氧化物对应水化物的碱性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、M、N是短周期主族元素,且原子序数依次增大。已知X的最外层电子数是电子层数的3倍,X、M同主族,Y的原子在短周期主族元素中原子半径最大。下列说法正确的是
A.M与X形成的化合物对应的水化物一定是强酸
B.Y2X和Y2X2中阴、阳离子的个数比相同,化学键类型也完全相同
C.X、Y的简单离子半径:r(X2-)>r(Y+)
D.M的气态氢化物比N的气态氢化物稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
柠檬酸铁可用作食品铁质强化剂、营养增补剂,用于饼干、钙质奶粉等,它可以由柠檬酸(熔点为153ºC)与氢氧化铁制得。其结构如右图。
(1)柠檬酸的晶体类型为 。
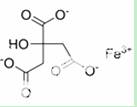 (2)柠檬酸铁中基态Fe3+的价电子排布式为 。
(2)柠檬酸铁中基态Fe3+的价电子排布式为 。
(3)柠檬酸铁所含非金属元素,电负性从小到大的顺序为
(填元素符号)。
(4)柠檬酸铁中,碳原子的杂化轨道类型为 。
(5)I2(Fe) I3(Fe)(填“>”或“<”)。
(6)柠檬酸铁溶液中不存在的微粒间作用力为 (填序号)。
A.离子键 B.极性键 C.非极性键
D.金属键 E.氢键 F.范德华力
(7)H3O+中H-O-H键角比H2O中H-O-H键角大,原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关硅及其化合物的说法错误的是( )
A.硅的导电性能介于导体和绝缘体之间,是良好的半导体材料
B.二氧化硅属于酸性氧化物,不能与任何酸反应
C.硅酸可通过可溶性硅酸盐与其他酸反应制得,硅酸酸性比碳酸弱
D.硅酸钠的水溶液俗称水玻璃,可作木材防火剂
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、w四种物质的转化关系如图所示(部分反应物和产物已经省略)。下列组合中不符合该关系的是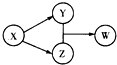
| A | B | C | D | |
| X | HCl | Na2O2 | Na2CO3 | SO2 |
| Y | FeCl2 | NaOH | CO2 | Na2SO3 |
| Z | Cl2 | Na2CO3 | CaCO3 | H2SO4 |
| W | FeCl3 | NaHCO3 | Ca(HCO3)2 | NaHSO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com