
���� ��1������m=CVM������Ҫ���ʵ���������ȡ��ʴ��ҩƷ��Ӧʢ����С�ձ��У�
��2����������һ�����ʵ���Ũ����Һ��һ�㲽��ѡ����Ҫ��������
��3�����ݣ�2����֪ȱ�ٲ����������ݲ������������ܽ⡢��Һ�����е����ý��
��4������ʱ���ò�����������������ˮ����̶�1��2 cm�������ý�ͷ�ι���εμӣ�ʹ��Һ��Һ�桢�̶��ߡ�������ƽ��
��5���ٸ���8gNaOH�����м���100mL����ˮ����Һ����ӽ�100mL�����������
�ڸ�����Ͳ���������ܽ���壻
�۸�������ƿ����ֱ�������ܽ���壻
�ܸ���������Һ�к������ʵ����ʵ����Ƿ�����жϣ�
��6���������������ʵ����ʵ�������Һ�����Ӱ�죬����C=$\frac{n}{V}$������������
��� �⣺��1���ù����ռ�����500mL 0.1mol•L-1��NaOH��Һ����Ҫ������������m=0.1mol/L��0.5L��40g/mol=2.0g���������ƾ��и�ʴ�ԣ�Ӧ����С�ձ��г�����
�ʴ�Ϊ��2.0�� С�ձ���
��2������һ�����ʵ���Ũ����Һ��һ�㲽�裺���㡢�������ܽ⡢��Һ��ϴ�ӡ����ݡ�ҡ�ȣ��õ���������������ƽ��ҩ�ס���ͷ�ιܡ��ձ�������������500mL��ƿ���ò�����������C��1000mL����ƿ��H��©����
��ѡ��C H��
��3�����ݣ�2����֪ȱ�ٲ����������ܽ�NaOHʱ���������NaOH�ܽ⡡ ת����Һʱ����������ֹҺ�彦ʧ��
�ʴ�Ϊ���������������ܽ�NaOHʱ���������NaOH�ܽ⡡ ת����Һʱ����������ֹҺ�彦ʧ��
��4�����ݵ���ȷ�������ò�����������������ˮ����̶�1��2 cm�������ý�ͷ�ι���εμӣ�ʹ��Һ��Һ�桢�̶��ߡ�������ƽ��
�ʴ�Ϊ���ò�����������������ˮ����̶�1��2 cm�������ý�ͷ�ι���εμӣ�ʹ��Һ��Һ�桢�̶��ߡ�������ƽ��
��5�����ʵ�����Ϊm=nM=cvM=2mol/L��0.1L��40g/mol=8g��
�ٸ���Ũ��ԼΪ2mol/L NaOH��Һ100mL�����Ǵ������ƣ����Կɽ�8g NaOH���壬����250mL�ձ��У���100mL��Ͳ��ȡ100mL����ˮ�������ձ��У�ͬʱ���Ͻ����������ܽ⣬����ȷ��
������Ͳ���������ܽ���壬�ʴ���
��������ƿ����ֱ�������ܽ���壬�ʴ���
��100mL2mol•L-1 ��NaOH��Һ�����������Ƶ����ʵ�����0.2mol��40mL5mol•L-1��NaOH��Һ�����������Ƶ����ʵ�����0.2mol��������Һ���ʵ����ʵ�����ȣ��������������ʵ���Ũ��ԼΪ2mol•L-1 NaOH��Һ100mL������ȷ��
��ѡ���٢ܣ�
��6��A������ʱ�����̸ߣ����̵ͣ����³�ȡ�����ʵ�����ƫС�����ʵ����ʵ���ƫС����ҺŨ��ƫ�ͣ���A��ѡ��
B������ʱ��������ƿ�̶��ߣ�������Һ���ƫС����ҺŨ��ƫ�ߣ���Bѡ��
C��ԭ����ƿϴ����û�и�������ʵ����ʵ�������Һ�����������Ӱ�죬��ҺŨ�Ȳ��䣬��C��ѡ��
D��ҡ�Ⱥ��Һ���½����ټ�ˮ���̶��ߵģ�������Һ���ƫ����ҺŨ��ƫ�ͣ���D��ѡ��
��ѡ��B��
���� ����������һ�����ʵ���Ũ����Һ���ƣ���ȷ����ԭ�������������ǽ���ؼ���ע������ƿ����Ͳ���ѡ��ʹ�÷�����ע�������Ŀ�ѶȲ���


 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �õ����ZnΪ������������ԭ��Ӧ | |
| B�� | �õ�ص�������ӦʽΪMnO2+e-+H2O=MnOOH+OH- | |
| C�� | ����ʱ���·������Zn����MnO2���ڵ�·������MnO2����Zn | |
| D�� | ��ع���ʱ�ڵ�·��OH-�ƶ���MnO2һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
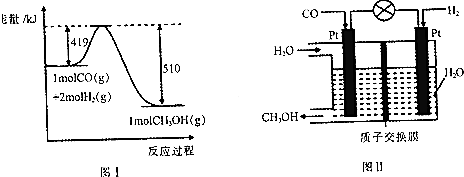
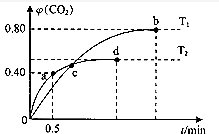
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ����� | ���� | ���ͻ���� |
| A | ��ij��Һ�м��������ữ��BaCl2��Һ | �а�ɫ�������� | ��Һ�в�һ������SO42- |
| B | ��װ��Fe��NO3��2��Һ�Թ��м���ϡH2SO4 | �ڹܿڹ۲쵽����ɫ���� | HNO3�ֽ����NO2 |
| C | ��CH3CH2X�м�������AgNO3��Һ������ | ��dz��ɫ�������� | CH3CH2X�к���Be+ |
| D | �������Һ�м���ϡH2SO4���ȼ����ӣ���ȴ���ټ�������Cu��OH��2��Һ������ | û�к�ɫ�������� | ����û��ˮ��������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �������� | HCl��aq�� | FeCl3 | NaOH | CH3COONa | C2H5OH |
| ��Һ��pH | 3 | 4 | 10 | 11 | δ�ⶨ |
| ˮ�ĵ���̶� | ��1 | ��2 | ��3 | ��4 | ��5 |
| A�� | ��3����1����5����4����2 | B�� | ��4����2����5����3����1 | C�� | ��2����4����5����1����3 | D�� | ��1����3����5����2����4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | -1 528.6kJ•mol-1 | B�� | -1 473kJ•mol-1 | ||
| C�� | +1 473 kJ•mol-1 | D�� | +1 528.6 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧʽ | ���볣����25�棩 |
| HCN | K=4.9��10-10 |
| CH3COOH | K=1.8��10-5 |
| H2CO3 | K1=4.3��10-7��K2=5.6��10-11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com