
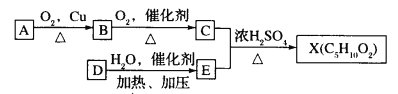
【题目】已知X的性质与乙酸乙酯相似,是一种具有果香味的合成香料,图为合成X的某种流程:
提示:①![]() 不能最终被氧化为一COOH;
不能最终被氧化为一COOH;
②D的产量可以用来衡量一个国家的石油化工水平。
请根据以上信息,回答下列问题:
(1)A的结构简式是_____。分子中官能团的名称是_______
(2)C + E一 X的化学反应类型为________。
(3)C的一种同分异构体F可以发生水解反应,则F的结构简式为_______
(4)反应D-E的化学方程式为__________
(5)与碳酸氢钠溶液反应生成CO2的X的同分异构体有_________
(6)为了制取X,某同学设计如下实验装置:
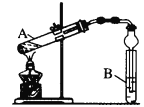
试管B中放入的试剂是_______装置中球形干燥管除起冷凝作用外,另一重要作用是_____
【答案】CH3CH2CH2OH 羟基 酯化反应(或取代反应) HCOOCH2CH3、CH3COOCH3 CH2=CH2+ H2O![]() CH3CH2OH 4 饱和碳酸钠溶液 防倒吸
CH3CH2OH 4 饱和碳酸钠溶液 防倒吸
【解析】
D的产量可以用来衡量一个国家的石油化工水平,D为乙烯;乙烯与水反应得到E为乙醇;X的性质与乙酸乙酯相似,是一种具有果香味的合成香料,X为酯类,则C应为丙酸;C由B氧化得到,可知B为丙醛;B由A氧化得到则A为丙醇,又![]() 不能最终被氧化为一COOH,可知A为1-丙醇,据此解答。
不能最终被氧化为一COOH,可知A为1-丙醇,据此解答。
(1) 根据以上分析,A为1-丙醇,结构简式为:CH3CH2CH2OH,所含官能团为羟基,故答案为:CH3CH2CH2OH;羟基;
(2) C + E一 X为乙醇与丙酸的酯化反应,酯化反应也属于取代反应,故答案为:酯化反应(或取代反应);
(3) C为丙酸其一种同分异构体F可以发生水解反应,则F应为酯类,有甲酸乙酯HCOOCH2CH3和乙酸甲酯CH3COOCH3
两种结构,故答案为:HCOOCH2CH3、CH3COOCH3;
(4)反应D-E为乙烯与水加成得到乙醇的反应,反应方程式为:CH2=CH2+ H2O![]() CH3CH2OH,故答案为:CH2=CH2+ H2O
CH3CH2OH,故答案为:CH2=CH2+ H2O![]() CH3CH2OH;
CH3CH2OH;
(5)与碳酸氢钠溶液反应生成CO2的X的同分异构体应含有羧基,相当于是丁烷上的氢被羧基取代,丁烷有正丁烷和异丁烷两种结构,每种结构中含两种氢,故符合条件的羧酸有4种,故答案为:4;
(6) 试管B中放入的试剂是饱和碳酸钠溶液,用于中和丙酸,溶解乙醇,降低丙酸乙酯的溶解度,便于其析出;装置中球形干燥管除起冷凝作用外,因乙醇、丙酸都易溶于水,导管通入溶液中时会引起倒吸,因此另一重要作用是防止倒吸,故答案为:饱和碳酸钠溶液;防倒吸;


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是( )


A. ①是其他条件一定时,反应速率随温度变化的图像,正反应ΔH<0
B. ②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图像
C. ③是在有无催化剂存在下建立的平衡过程图像,a是使用催化剂时的曲线
D. ④是一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强p1>p2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,向l0mL0.01mol·L-1NaA溶液中逐滴加入0.01mol·L-1的盐酸,滴定曲线如下图所示,下列说法正确的是( )

A. a点到c点的过程中,c(HA)+c(A-)=0.01mol·L-1等式始终成立
B. b点时,溶液中微粒浓度大小的关系:c(A-)>c(Cl-)>c(HA)>c(OH-)>c(H+)
C. c点溶液存在的关系:c(Na+)+c(H+)=c(HA)+c(OH-)+2c(A-)
D. 由图可知,等浓度的HA、NaA混合溶液中,HA的电离程度大于A-的水解程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.常温下,加水稀释氨水,稀释过程中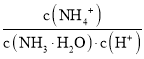 的值不变
的值不变
B.反应NH3(g)+HCl(g)=NH4Cl(s) △H<0在任何条件下均能自发进行
C.常温下电解CuSO4溶液,产生22.4LO2,反应中转移的电子数为4×6.02×1023个
D.为防止浸泡在海水中的闸门腐蚀,可以在闸门上焊接铜块
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有容积相同的4个集气瓶,分别装满下列各气体,倒扣在盛水的水槽中,经充分反应后,集气瓶进水最多的是
A.NO和N2体积各占50%B.NO2和N2体积各占50%
C.NO2和O2体积各占50%D.NO和O2体积各占50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A、E在元素周期表中的相对位置如图,A与氧元素能形成两种无色气体,C是地壳中含量最多的元素,D是地壳中含量最多的金属元素。
A | ||
E |
(1)C在元素周期表中的位置为____。
(2)AE2的电子式为___。
(3)C、E、F的单质沸点最低的是__(填化学式)。
(4)C、D、E、F的离子半径由大到小的顺序是___(填离子符号)。
(5)实验室制取F2气体的离子方程式为___。
(6)在微电子工业中,B的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在一容积不变的密闭容器中发生可逆反应2X(g)![]() Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是
Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是
A.混合气体的密度不再变化B.反应容器中Y的质量分数不变
C.体系压强不再变化D.c(X):c(Y):c(Z)=2:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物Z是制备药物的中间体,合成Z的路线如图所示:
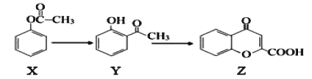
下列有关叙述正确的是( )
A.Y分子中所有原子可能处于同一平面
B.X、Y、Z均能和Na2CO3溶液反应
C.Y、Z都可能使浓溴水褪色,反应原理不相同
D.1molZ跟足量H2反应,最多消耗6molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙各取300 mL同浓度的盐酸,加入不同质量的同一镁铝合金粉末进行下列实验,有关数据列表如下:
实验序号 | 甲 | 乙 | 丙 |
合金质量/mg | 510 | 765 | 918 |
(标准状况)气体体积/mL | 560 | 672 | 672 |
求:(1)盐酸的物质的量浓度是多少________?
(2)合金中镁铝的质量分数各是多少________?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com