
【题目】过碳酸钠和盐酸反应的化学方程式为:2Na2CO4+4HCl=4NaCl+2CO2↑+O2↑+2H2O,商品过碳酸钠中一般都含有Na2CO3,为了测定它的纯度,取一定量的样品和盐酸反应,通过测量产生的氧气的体积,可以计算出过碳酸钠的含量。
(1) 根据下图提供的仪器装置,组装一套测定商品过碳酸钠的实验装置,这些装置的连接顺序是(填接口字母):_______________。

(2) 装置④的作用:______________________。装置⑤的作用为_________________________________。
(3) 如果实验时,称取wg样品和过量盐酸反应后,设收集到氧气的体积(标准状况)为VmL,则此样品的纯度为______________。(列出计算式,不需化简)
(4) 某次实验,称取1.22g样品进行测定,实验室有50mL,100mL,150mL三种规格的量筒,应选用规格为_______的量筒进行实验。
【答案】(1)aghefdcb(2)检验CO2是否已除净
(3)![]() (4)100mL
(4)100mL
【解析】
试题(1)过碳酸钠和碳酸钠均能与足量的盐酸反应,放出含有CO2和O2的气体,CO2对O2体积测量有干扰,因此利用排水量气法收集O2之前,需要除去CO2并确认CO2已经被完全除尽;图中几个装置的作用分别是制气、量液或O2的体积、排水集O2、确认是否含有CO2、除去CO2,除去并检验CO2时气体应该长进短出,排水集O2时应短进长出,因此这套装置的连接顺序为a→g,h→e,f→d,c→b;
(2)根据以上分析可知装置④的作用是检验CO2是否已除净;
(3)先由n=V/Vm求 n(O2),再由反应式2Na2CO4+4HCl=4NaCl+2CO2↑+O2↑+2H2O中过碳酸钠与氧气的化学计量数之比等于物质的量之比求 n(Na2CO4),然后再由m=nM求m(Na2CO4),最后由过碳酸钠的质量和样品的质量求纯度,即纯度为![]() 。
。
(4)根据方程式可知0.9g样品最多生成氧气的体积是![]() ,所以需要100mL量筒。
,所以需要100mL量筒。


科目:高中化学 来源: 题型:
【题目】某同学拟用煤干馏的产物W为基本原料合成一系列化工产品,其流程如下(部分产物和条件省略):

己知部分信息如下:
①1mol芳香烃W含50mol电子;
②![]() ;
;
③![]() (苯胺,易被氧化)
(苯胺,易被氧化)
④K的分子式为C7H6O2,其核磁共振氢谱上有4个峰。
请回答下列问题:
(1)X的名称为_________,Y中所含官能团的名称为_________ 。
(2)反应⑦的条件为_________,②的反应类型________。
(3)反应⑤的化学方程式为_________。
(4)Z的结构简式为_________ 。
(5)K的同分异构体M既能发生水解反应,又能发生银镜反应,M在氢氧化钠溶液中发生水解反应的化学方程式为__________。
(6) 有多种同分异构体,写出符合以下3个条件的同分异构体的结构简式_________。
有多种同分异构体,写出符合以下3个条件的同分异构体的结构简式_________。
①能发生银镜反应但不能水解。
②每摩尔同分异构体最多消耗2molNaOH。
③苯环上一氯代物只有两种。
(7)请以流程图的形式写出由T制备 的过程(无机试剂任选):(仿照
的过程(无机试剂任选):(仿照 )_____________________
)_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用短线“—”表示共用电子对,用“··”表示未成键孤电子对的式子叫路易斯结构式。R分子的路易斯结构式可以表示为![]() 则以下叙述错误的是( )
则以下叙述错误的是( )
A. R为三角锥形 B. R可以是BF3
C. R是极性分子 D. 键角小于109°28′
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q为短周期非金属元素,R是长周期元素。X原子的电子占据2个电子层且原子中成对电子数是未成对电子数的2倍;Y的基态原子有7种不同运动状态的电子;Z元素在地壳中含量最多;Q是电负性最大的元素;R+只有三个电子层且完全充满电子。
请回答下列问题:(答题时,X、Y、Z、Q、R用所对应的元素符号表示)
(1)R的基态原子的电子排布式为________。
(2)X、Y、Z三种元素第一电离能从大到小顺序为______________________。
(3)已知Y2Q2分子存在如下所示的两种结构(球棍模型,短线不一定代表单键):

①该分子中两个Y原子之间的键型组合正确的是________。
A.仅1个σ键
B.1个σ键和2个π键
C.1个σ键和1个π键
D.仅2个σ键
②该分子中Y原子的杂化方式是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚烷(Ⅰ)、乙二醛、丙二醛均是化工原料,某小组设计的合成路线如下:
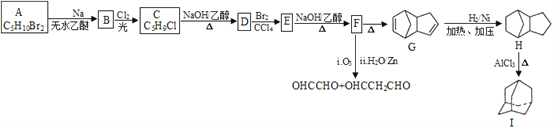
已知:
①2R-Br+2Na![]() R-R+2NaBr
R-R+2NaBr
②B的核磁共振氢谱只有1个吸收峰
③![]()
④![]()
回答下列问题:
(1)A的化学名称为_____________; D的结构简式为__________________;I的分子式为__________________。
(2)B→C的化学方程式_________________;E→F的化学方程式为_______________。该反应类型为________________。
(3)G的芳香族同分异构体中,苯环上的取代基数目小于3且能使溴的四氯化碳溶液褪色的共有_______种(不含立体异构);其中核磁共振氢谱有5组峰,且峰面积比为6:2:2:1:1的是_________________(写结构简式)。
(4)写出用环戊二烯和乙烯为原料制备化合物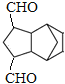 的合成路线____________(其他试剂任选)。
的合成路线____________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e、f、g为七种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下所示:(单位:电荷)
粒子代号 | a | b | c | d | e | f | g |
原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
电荷数 | |||||||
(单位电荷) | 0 | +1 | -1 | 0 | +2 | +1 | 0 |
其中b的离子半径大于e的离子半径;c与f可形成两个共价型g分子。
试写出:
(1)a粒子的原子结构示意图是________;b粒子的电子排布式为________。
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为________(用化学式表示)。
(3)若d极易溶于水,在水溶液中变化的方程式为________,d分子的空间构型为________,键角为________;若d为正四面体形分子,其电子式为________。
(4)c粒子是________,f粒子是________(用化学式表示),由c、f生成g的离子方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液分别滴定浓度均为0.10mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示。下列判断不正确的是
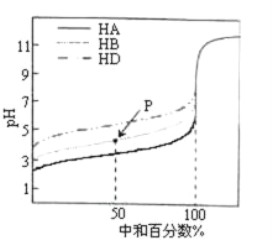
A. 三种酸的电离平衡常数:K(HA)>K(HB)>K(HD)
B. 滴定至M点时,溶液中:c(B-)>c(Na+)>c(HB)>cH+)>c(OH-)
C. pH=7时,三种溶液中:c(A-)>c(B-)>c(D-)
D. 当中和百分数达到100%时,三种溶液中:c(HA)>c(HB)>c(HD)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.用苯萃取碘水中的碘,后分液,水层从上口倒出
B.金属氧化物都是碱性氧化物
C.三氯化铁溶液滴入氢氧化钠溶液可制备氢氧化铁胶体
D.可用量筒准确量取9.5mL水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com