
| 实验编号 | 待测血液的体积/mL | 滴入KMnO4溶液的体积/mL |
| 1 | 20.00 | 11.95 |
| 2 | 20.00 | 13.00 |
| 3 | 20.00 | 12.05 |
| 5 |
| 2 |
| 0.024g |
| 20cm3 |


科目:高中化学 来源:不详 题型:多选题
| A.可以用FeCl3溶液区别出苯酚溶液、乙醇、苯 |
| B.向淀粉溶液中加入少量稀硫酸,加热一段时间后,加入新制的Cu(OH)2悬浊液,加热,无砖红色沉淀生成,则说明淀粉未发生水解 |
| C.判断油脂皂化反应基本完成的方法是用胶头滴管吸取少量混合液体加入到蒸馏水中,未发生分层现象,则说明油脂皂化反应基本完成 |
| D.电解精炼铜的实验中,当阴极流入2mol电子时,阳极溶解了64gCu |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该溶液中阳离子只有钾离子 |
| B.该溶液中一定含有钠离子 |
| C.该溶液中可能含有钠离子,但一定含有钾离子 |
| D.该溶液中可能含有钾离子,但一定含有钠离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
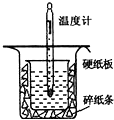
| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | ______ |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 实验编号 | 邻苯二甲酸氢钾的质量(g) | 待测NaOH溶液的体积(mL) |
| 1 | 0.4162 | 18.25 |
| 2 | 17.04 | |
| 3 | 16.96 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.石蕊、由蓝变红 | B.酚酞、红色褪去 |
| C.甲基橙,由橙变黄 | D.甲基橙、由黄变橙 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| V(HCl)/mL | 0.00 | 12.00 | 18.00 | 22.00 | 23.00 | 23.96 | 24.00 | 24.04 | 25.00 | 26.00 | 30.00 |
| pH | 13.1 | 12.6 | 12.2 | 11.7 | 11.4 | 9.9 | 7.0 | 4.0 | 2.7 | 2.4 | 1.9 |
| 指示剂 | 变色范围 (pH) | 各范围内颜色 | ||
| 前 | 中间 | 后 | ||
| 甲基橙 | 3.1~4.4 | 红 | 橙色 | 黄 |
| 石蕊 | 5.0~8.0 | 红 | 紫色 | 蓝 |
| 酚酞 | 8.2~10.0 | 无 | 粉红 | 红 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 滴定次数 | NaOH溶液体积(mL) | |
| V1 | V2 | |
| 1 | 3.05 | 44 |
| 2 | 1.45 | 41.5 |
| 3 | 7.65 | 47.6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.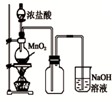 如图中:即使MnO2过量,盐酸也不能全部消耗 |
B. 如图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |
C.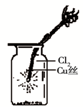 如图中:生成棕色的烟 |
D.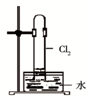 如图中:水可以充满试管 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com