
| A、0.1 mol?L-1的CH3COOH溶液中,由水电离的c(H+)为10-13mol?L-1 |
| B、pH=2与pH=1的CH3COOH溶液中c(H+)之比为1:10 |
| C、pH=12的NaOH溶液和pH=2的CH3COOH溶液等体积混合后溶液的pH<7 |
| D、将1 L 0.1 mol?L-1的Ba(OH)2溶液稀释为2 L,pH=13 |
| 0.1mol/L×2×1L |
| 2L |


科目:高中化学 来源: 题型:
| A、N2(O2):通过灼热的镁粉 |
| B、SiO2(Fe2O3):足量的盐酸,过滤 |
| C、CO2(SO2):酸性KMnO4溶液、浓硫酸,洗气 |
| D、C2H5OH(CH3COOH):加足量CaO,蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
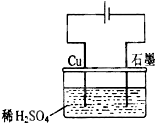
| A、电解过程中,铜电极上有H2产生 |
| B、电解过程中,铜电极不断溶解 |
| C、电解过程中,石墨电极上始终有铜析出 |
| D、整个电解过程中,H+的浓度不断增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
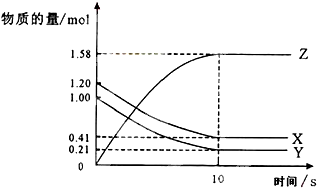 一定温度下,在2L的密闭容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示下列描述正确的是( )
一定温度下,在2L的密闭容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示下列描述正确的是( )| A、反应开始到10 s,用Z表示的反应速率为0.158 mol/(L?s) |
| B、反应开始到10 s,X的物质的量浓度减少了0.79 mol/L |
| C、反应开始到10 s时,Y的转化率为79% |
| D、反应的化学方程式为:X(g)+Y(g)?Z(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:
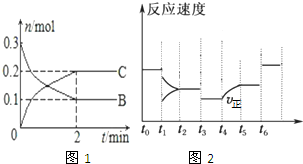
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com