
在稀硫酸酸化的H2O2溶液中加入乙醚(C2H5 —O—C2H5 )后,溶液分层,再加入少量K2Cr2O7 溶液,并振荡,在乙醚层中出现深蓝色,这是因为生成2CrO5?(C2H5)2O所致,其反应方程式为:Cr2O72- +
4H2O2+2H+ = 2CrO5 + 5H2O
,已知:CrO5 的结构式为: 下列说法正确的是
下列说法正确的是
A.Cr2O72-被氧化成CrO5 B.该反应为氧化还原反应
C.反应中H2O2被还原成H2O D.此反应用于检验Cr2O72-离子的存在
科目:高中化学 来源: 题型:阅读理解



查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:


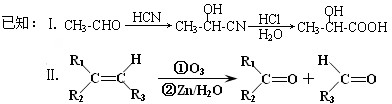
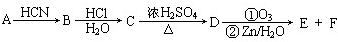
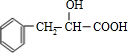
| 浓硫酸 |
| △ |
 +H2O
+H2O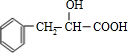
| 浓硫酸 |
| △ |
 +H2O
+H2O
| 一定条件 |
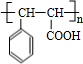

| 一定条件 |



查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com