
| A. | 35Cl和37Cl的原子结构示意图均为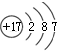 | |
| B. | HCI的形成过程为 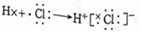 | |
| C. | 乙烯的结构简式为CH2CH2 | |
| D. | 草酸的电离过程为H2C2O4?2H++C2O42- |
分析 A.两种微粒都是氯原子,其原子结构示意图相同;
B.氯化氢为共价化合物,分子中不存在阴阳离子;
C.乙烯的结构简式中必须标出碳碳双键;
D.草酸为二元弱酸,其电离方程式需要分步书写.
解答 解:A.35Cl和37Cl核电荷数、核外电子总数都是17,二者的原子结构示意图均为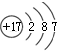 ,故A正确;
,故A正确;
B.HCl为共价化合物,电子式中不能标出阴阳离子,用电子式表示其形成过程为 ,故B错误;
,故B错误;
C.乙烯分子中含有碳碳双键,其正确的结构简式为:CH2=CH2,故C错误;
D.草酸的电离分步进行,主要以第一步为主,正确的电离方程式为:H2C2O4?H++HC2O4-,故D错误;
故选A.
点评 本题考查常见化学用语的表示方法,题目难度不大,涉及原子结构示意图、电子式、结构简式、电离方程式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | Na和Na+ | B. | 35Cl和37Cl | ||
| C. | 14N和 14C | D. | ${\;}_{8}^{16}$O2和${\;}_{8}^{18}$O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
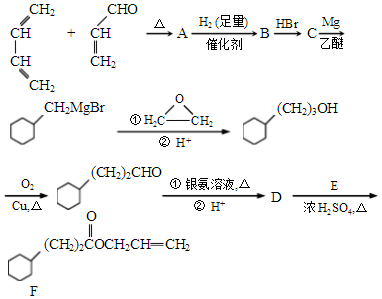
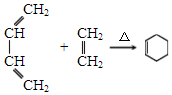
 ,A中所含官能团的名称是醛基、碳碳双键.
,A中所含官能团的名称是醛基、碳碳双键. .
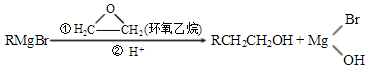
.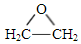 )为原料制备1丁醇,设计合成路线
)为原料制备1丁醇,设计合成路线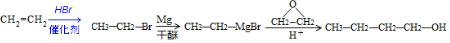 (其它试剂任选).(合成路线常用表示方法为:A $→_{反应条件}^{反应试剂}$ B …$→_{反应条件}^{反应试剂}$目标产物)
(其它试剂任选).(合成路线常用表示方法为:A $→_{反应条件}^{反应试剂}$ B …$→_{反应条件}^{反应试剂}$目标产物)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L氢氧化钠溶液 | B. | 0.1mol/L氢氧化钡溶液 | ||
| C. | 0.1mol/L氢氧化钾溶液 | D. | 0.1mol/L氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10% | B. | 11.1% | C. | 0.1% | D. | 20% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 同分异构体的结构简式.
同分异构体的结构简式.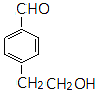 、
、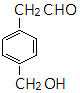 .
.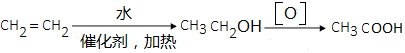 .(无机试剂可以任选)
.(无机试剂可以任选)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 编号 | A(KMnO4溶液浓度/mol•L-1) | B(草酸溶液浓度/mol•L-1) | C(硫酸溶液浓度/mol•L-1) | 褪色时间/s |
| 1 | 3 | 3 | 1 | 336 |
| 2 | 1 | 2 | 3 | 82 |
| 3 | 3 | 1 | 3 | 76 |
| 4 | 1 | 3 | 2 | 133 |
| 5 | 2 | 3 | 3 | 102 |
| 6 | 3 | 2 | 2 | 156 |
| 7 | 2 | 2 | 1 | 300 |
| 8 | 2 | 1 | 2 | 115 |
| 9 | 1 | 1 | 1 | 200 |
| A(KMnO4溶液) | B(草酸溶液) | C(硫酸溶液) | |||||||
| 浓度/mol•L-1 | 0.005 | 0.010 | 0.015 | 0.1 | 0.5 | 0.9 | 6 | 12 | 18 |
| 平均褪色时间/s | 138.3 | 172.3 | 189.3 | 130.3 | 179.3 | 190.3 | 278.7 | 134.7 | 86.7 |
| c(H2SO4)/mol•L-1 | 18 | 16 | 14 | 12 | 10 | 8 | 6 |
| 褪色时间/s | 67 | 83 | 90 | 103 | 129 | 146 | 200 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使甲基橙变红的溶液中:Fe2+、Al3+、NO3-、Cl- | |
| B. | 在pH=12的溶液中:Na+、AlO2-、NO3-、S2- | |
| C. | 室温下,由水电离的c(H+)=10-10mol/L的溶液中:Cl-、HCO3-、NO3-、NH4+ | |
| D. | 加入Mg能放出H2的溶液中:Mg2+、NH4+、ClO-、K+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com