
实验室利用下列装置和试剂制取少量氯化氢气体.

试剂:①浓硫酸;②浓盐酸;③食盐固体;④硫酸氢钠固体;⑤二氧化锰固体.
请用实验装置编号(A、B……)完成下列问题:
(1)若选用试剂①③,则应选择的装置是________.
(2)若选用试剂③④,则应选择的装置是________.
(3)若要快速制备氯化氢,应选择的装置是________.
科目:高中化学 来源: 题型:

试剂:①浓硫酸;②浓盐酸;③食盐固体;④硫酸氢钠固体;⑤二氧化锰固体。
请用实验装置编号(A、B……)完成下列问题:
(1)若选用试剂①③,则应选择的装置是__________________________。
(2)若选用试剂③④,则应选择的装置是__________________________。
(3)若要快速制备氯化氢,应选择的装置是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(16分)黄铁矿的主要成分是FeS2。测定黄铁矿中FeS2含量的两种方法如下图所示:
已知:①王水是由1体积的浓硝酸(ρ=1.42g·cm-3)和3体积的浓盐酸(ρ=1.19g·cm-3)混合而成的。
②黄铁矿和王水反应的方程式为FeS2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O
请回答下列问题:
(1)简述实验室配制王水的操作过程_____________________________________
________________________________________________________________。
(2)方法一中过滤、洗涤、灼烧都用到的仪器是_______________。
(3)方法二中要判断BaCl2溶液是否过量,可向滤液中加入X溶液,X可以是_________(填代号)
A.BaCl2 B.NaOH C.Na2SO4 D.HCl
(4)实验室利用下列装置和试剂制取少量氯化氢气体试剂:①浓硫酸 ②浓盐酸 ③食盐固体
若选用试剂①③,则应选择的装置是___________(填代号,下同);推测发生反应的化学方程式为__________________________________________________;
若选用试剂①②,则宜选择的装置是____________。
(5)方法一中,灼烧时发生反应的化学反应方程式为________________________;已知称取黄铁矿样品的质量为1.50g,称得灼烧后固体的质量为0.8g,不考虑操作误差,则该矿石中FeS2的质量分数是________________。
查看答案和解析>>
科目:高中化学 来源:2010年山东省威海市高三第二次模拟考试(理科综合)化学部分 题型:实验题
(16分)黄铁矿的主要成分是FeS2。测定黄铁矿中FeS2含量的两种方法如下图所示:
已知:①王水是由1体积的浓硝 酸(ρ=1.42g·cm-3)和3体积的浓盐酸(ρ=1.19g·cm-3)混合而成的。
酸(ρ=1.42g·cm-3)和3体积的浓盐酸(ρ=1.19g·cm-3)混合而成的。
②黄铁矿和王水反应的方程式为FeS2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O
请回答下列问题:
(1)简述实验室配制王水的操作过程_____________________________________
________________________________________________________________。
(2)方法一中过滤、洗涤、灼烧都用到的仪器是_______________。
(3)方法二中要判断BaCl2溶液是否过量,可向滤液中加入X溶液,X可以是_________(填代号)
| A.BaCl2 | B.NaOH | C.Na2SO4 | D.HCl |

查看答案和解析>>
科目:高中化学 来源:2011-2012学年辽宁省高三上学期第三次月考化学试卷 题型:实验题
黄铁矿的主要成分是FeS2。测定黄铁矿中FeS2含量的两种方法如下图所示:
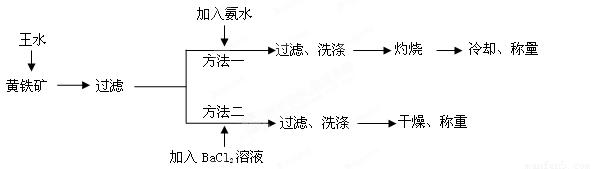
已知:
①王水是由1体积的浓硝酸(ρ=1.42g·cm-3)和3体积的浓盐酸(ρ=1.19g·cm-3)混合而成的。
②黄铁矿和王水反应的方程式为FeS2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O
请回答下列问题:
(1)简述实验室配制王水的操作过程_____________________________________
(2)方法一中过滤、洗涤、灼烧都用到的仪器是_______________。
(3)方法二中要判断BaCl2溶液是否过量,可向滤液中加入X溶液,X可以是____(填代号)
A.NaOH B.BaCl2 C.HCl D. Na2SO4
(4)实验室利用下列装置和试剂制取少量氯化氢气体
试剂:①浓硫酸 ②浓盐酸 ③食盐固体
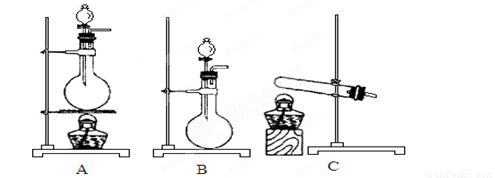
若选用试剂①②,则宜选择的装置是____________。
若选用试剂①③,则应选择的装置是___________(填代号,下同);推测发生反应的化学方程式为__________________________________________________;
(5)方法一中,灼烧时发生反应的化学反应方程式为________________________ ;已知称取黄铁矿样品的质量为1.50g,称得灼烧后固体的质量为0.4g,不考虑操作误差,则该矿石中FeS2的质量分数是________________。
查看答案和解析>>
科目:高中化学 来源:2010年山东省威海市高三第二次模拟考试(理科综合)化学部分 题型:实验题
(16分)黄铁矿的主要成分是FeS2。测定黄铁矿中FeS2含量的两种方法如下图所示:

已知:①王水是由1体积的浓硝酸(ρ=1.42g·cm-3)和3体积的浓盐酸(ρ=1.19g·cm-3)混合而成的。
②黄铁矿和王水反应的方程式为FeS2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O
请回答下列问题:
(1)简述实验室配制王水的操作过程_____________________________________
________________________________________________________________。
(2)方法一中过滤、洗涤、灼烧都用到的仪器是_______________。
(3)方法二中要判断BaCl2溶液是否过量,可向滤液中加入X溶液,X可以是_________(填代号)
A.BaCl2 B.NaOH C.Na2SO4 D.HCl
(4)实验室利用下列装置和试剂制取少量氯化氢气体试剂:①浓硫酸 ②浓盐酸 ③食盐固体
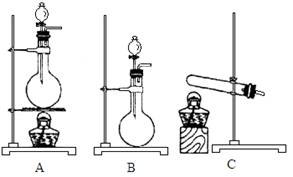
若选用试剂①③,则应选择的装置是___________(填代号,下同);推测发生反应的化学方程式为__________________________________________________;
若选用试剂①②,则宜选择的装置是____________。
(5)方法一中,灼烧时发生反应的化学反应方程式为________________________ ;已知称取黄铁矿样品的质量为1.50g,称得灼烧后固体的质量为0.8g,不考虑操作误差,则该矿石中FeS2的质量分数是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com