
| ʵ�� | ���� | ���� |
| A | 1��0.2mol/LNaOH��Һ | ����ɫ |
| B | 1��ˮ | ������dz�غ�ɫ |
| C | 1��0.1mol/L������Һ | Ѹ�ٱ��غ�ɫ |

���� ��1�����������Ӻ�KSCN��Һ��Ӧ��Fe3++3SCN-?Fe��SCN��3��ɫΪѪ��ɫ�������ᱵΪ��ɫ����������������ϡ�����ڳ����²���Ӧ��
��2���ⵥ����ˮ�е���ɫΪ�غ�ɫ�����������������������ɵ��ʵ⣬��Ũ��Խ����ɫԽ������̵������Ժ͵����ӵĻ�ԭ�Խ��
��3������ʵ������IJ����Լ�ÿ��������Ҫ����ȷ����Ӧ������������������30%��H2O2��Һ��Ũ����3%��H2O2��Һ�Ĺ�ϵȷ���������Ͳ�������
��4��Ҫ̽����Ӧ����I2���˴�H2O2�ֽ�����ã�������˫��ˮ�м���ⵥ�ʣ�
��5������Ũ����Ͷ������̵�װ����ѡ��������
��6�����ݵ�ط�Ӧ��ԭ�����Ԫ�ػ��ϼ۽��͵�������������ԭ��Ӧ��
��� �⣺��1��A����MnO2������뵽FeSO4��Һ�У�����������̾��������ԣ���+2�۵���������+3�۵��������ټ���KSCN��Һ�����������Ӻ�KSCN��Һ��Ӧ��Fe3++3SCN-?Fe��SCN��3��ɫΪѪ��ɫ�����Թ۲���Һ�Ƿ�����жϣ���A��ȷ��
B����MnO2������뵽FeCl3��Һ�У��ټ���KSCN��Һ���۲���Һ�Ƿ��죬����MnO2����Ҳ�ܱ�죬��������������Ӻ�KSCN��Һ��Ӧ�Ľ������B����
C����Na2SO3��Һ�ټ���BaCl2��Һ���а�ɫ���������������ɣ�MnO2�����������أ���C����
D����MnO2������뵽ϡ�����У��۲��Ƿ��л���ɫ�������ɣ���Ӧ����I2���˴�H2O2�ֽ������ϡ�����ҳ��£�����Ӧ����D����
��ѡA��
��2���ٸ�С��������Ա�ʵ���У���Ũ��Խ����ɫԽ�˵�����ɵĵ�Խ�࣬��˶�Ӧ������������ǿ��
������������MnO2����I-���������̱���ԭ��+2�۵������ӣ������ӱ���ԭ�ɵ��ʵ⣬�������ӷ���ʽΪ��2I-+MnO2+4H+�TI2+Mn2++2H2O��
�ʴ�Ϊ������Խǿ��MnO2������Խǿ��2I-+MnO2+4H+�TI2+Mn2++2H2O��
��3�����Ʋ����м��㡢�������ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȵȲ�������30%��H2O2��Һ���ܶȰ�1g/cm3������Ũ��Ϊ3%��H2O2��Һ���ܶȰ�1g/cm3��100mL�����������Ũ��Ϊԭ����$\frac{1}{10}$����Ͳ�ľ�ȷ��Ϊ0.1mL������������Ͳ10.0mL��ȡҩƷ�����ձ����ܽ⣬��ȴ��
�ʴ�Ϊ��10.0���ձ���
��4��Ҫ̽����Ӧ����I2���˴�H2O2�ֽ�����ã�������˫��ˮ�м���ⵥ�ʣ����Ƿ��������弴�ɣ�
�ʴ�Ϊ��ȡ5mL3%��H2O2��Һ���Թ��У�����1�ε�ˮ���۲��Ƿ��д������ݲ���������˵��������ȷ����֮���費��ȷ��
��5��Ũ����Ͷ��������ڼ����������ܷ���������ԭ��Ӧ�����Ȼ��̡�������ˮ�����Թ�ѡ����ܼ��ȵķ�Ӧ������Բ����ƿ����Ӳ���Թܣ�
�ʴ�Ϊ��AD��
��6��MnO2�����������ɵ�أ�����ܷ�ӦΪ��Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O�����������ĵ缫��ӦʽΪ2MnO2+2NH4++2e-=Mn2O3+2NH3+H2O��
�ʴ�Ϊ��2MnO2+2NH4++2e-=Mn2O3+2NH3+H2O��
���� ������һ�����ʵ�����ʵ�鷽������⣬����ѧ�������ͽ�������������ע��֪ʶ��Ǩ�ƺ�Ӧ���ǹؼ����ѶȽϴ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
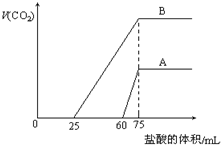 ȡ�����ݵ�Ũ�ȵ�NaOH��ҺA��B��ÿ��10mL���ֱ���A��B��ͨ�벻������CO2���ټ���������Һ����μ���0.2mol/L�����ᣬ��״���²�����CO2������������ӵ�������Һ���֮��Ĺ�ϵ��ͼ��ʾ���Իش��������⣺
ȡ�����ݵ�Ũ�ȵ�NaOH��ҺA��B��ÿ��10mL���ֱ���A��B��ͨ�벻������CO2���ټ���������Һ����μ���0.2mol/L�����ᣬ��״���²�����CO2������������ӵ�������Һ���֮��Ĺ�ϵ��ͼ��ʾ���Իش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
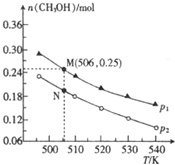 ����Ȼ��Ϊԭ�Ϻϳɼ״������ķ�����ˮú������Ŀǰ���ڿ�����ֱ����������
����Ȼ��Ϊԭ�Ϻϳɼ״������ķ�����ˮú������Ŀǰ���ڿ�����ֱ�����������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
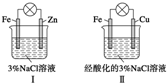
| A�� | ���в����γ�ԭ��� | |
| B�� | ���и�����Ӧ��Fe-3e-�TFe3+ | |
| C�� | ����������Ӧ��O2+2H2O+4e-�T4OH- | |
| D�� | ���м�������K3[Fe��CN��6]��Һ������ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Q1+Q2��Q3 | B�� | Q1+Q2��2Q3 | C�� | Q1+Q2��Q3 | D�� | Q1+Q2=Q3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��B��
��B�� ��C��
��C�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������ܽ���ˮ������������Һ��PM2.5�������ж����ЧӦ | |
| B�� | ������Ư�۳���������ˮ�Ĵ��������ߵ�����ԭ����ͬ | |
| C�� | �Ȼ�����Һ����������ӡˢ��·������Ϊ����н�ǿ�����ԣ���ͭ�����û���Ӧ | |
| D�� | ������ɱ�����в�������Ϊ���ɲ����ĵ��������ȱ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
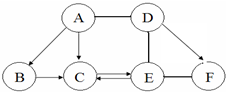 ��ͼ A��B��C��D��E��FΪ���л�ѧ���������ֺ��������A��B��C ��������Ԫ����ɣ��ڳ�����״̬������ͬ������AΪ��ɫ��ĩ��D��E��F ��������Ԫ����ɣ���������������ͬ����������ʾ���ʼ��ת����ϵ����-����ʾ�������������Ӧ�����ַ�Ӧ������P��Ӧ����δ��������ش��������⣺
��ͼ A��B��C��D��E��FΪ���л�ѧ���������ֺ��������A��B��C ��������Ԫ����ɣ��ڳ�����״̬������ͬ������AΪ��ɫ��ĩ��D��E��F ��������Ԫ����ɣ���������������ͬ����������ʾ���ʼ��ת����ϵ����-����ʾ�������������Ӧ�����ַ�Ӧ������P��Ӧ����δ��������ش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com