
【题目】沙罗特美是一种长效平喘药,其合成的部分路线如下:
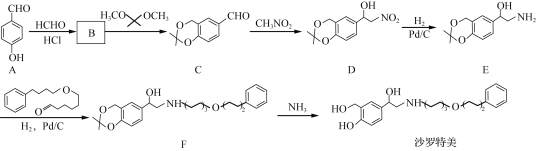
(1)F中的含氧官能团名称为____________(写两种)。
(2)C→D的反应类型为____________。
(3)B的分子式为C8H8O3,与(CH3)2C(OCH3)2发生取代反应得到物质C和CH3OH,写出B的结构简式:________。
(4)写出同时满足下列条件的E的一种同分异构体的结构简式:__________。
①分子中含有苯环,且有一个手性碳原子,不能与FeCl3发生显色反应;
②能发生水解反应,水解产物之一是α氨基酸,另一含苯环的水解产物分子中只有3种不同化学环境的氢。
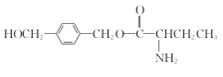
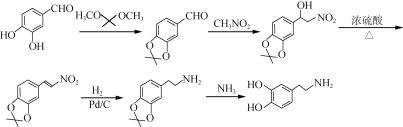
(5)请写出以 、(CH3)2C(OCH3)2、CH3NO2为原料制备
、(CH3)2C(OCH3)2、CH3NO2为原料制备 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干) _____。
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干) _____。
【答案】醚键 羟基 加成反应 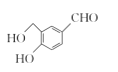
【解析】
(1)F的结构简式为: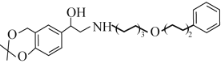 ,其中含氧官能团名称为醚键 羟基,
,其中含氧官能团名称为醚键 羟基,
故答案为:醚键 羟基;
(2)从流程图中可以看出,C→D,其醛基碳氧双键断裂,加氢还原的过程,无小分子出现,故该反应类型为:加成反应;
故答案为:加成反应;
(3)B的分子式为C8H8O3,含有不饱和度 = ![]() = 5,得到物质C和CH3OH,采用逆合成分析法可知,B的分子内含有两个羟基能与(CH3)2C(OCH3)2发生取代反应,则其结构简式为
= 5,得到物质C和CH3OH,采用逆合成分析法可知,B的分子内含有两个羟基能与(CH3)2C(OCH3)2发生取代反应,则其结构简式为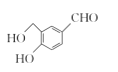 ,
,
故答案为: ;
;
(4)根据E的结构简式可知E的分子式为:C12H17NO3,含有不饱和度 = ![]() = 5,其同分异构体中,①分子中含有苯环,且有一个手性碳原子,不能与FeCl3发生显色反应,则苯环上没有酚羟基,结构中有一个碳原子周围连接四个不同的基团或原子;②能发生水解反应,水解产物之一是α氨基酸,则该同分异构体的结构中有肽键或者酯基,又另一含苯环的水解产物分子中只有3种不同化学环境的氢,则分子的对称性很好,综上同时符合上述两种条件的物质的结构简式为:
= 5,其同分异构体中,①分子中含有苯环,且有一个手性碳原子,不能与FeCl3发生显色反应,则苯环上没有酚羟基,结构中有一个碳原子周围连接四个不同的基团或原子;②能发生水解反应,水解产物之一是α氨基酸,则该同分异构体的结构中有肽键或者酯基,又另一含苯环的水解产物分子中只有3种不同化学环境的氢,则分子的对称性很好,综上同时符合上述两种条件的物质的结构简式为: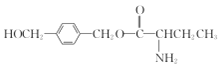 ,
,
故答案为: ;
;
(5)因酚羟基已被氧化,可考虑先制得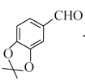 ,再引入硝基,最后再还原为羟基的思路,根据已知的流程图可推知,若要制备
,再引入硝基,最后再还原为羟基的思路,根据已知的流程图可推知,若要制备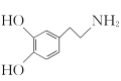 ,则需将
,则需将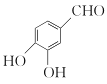 与(CH3)2C(OCH3)2发生取代反应得到
与(CH3)2C(OCH3)2发生取代反应得到 ,再与CH3NO2反应得到
,再与CH3NO2反应得到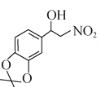 ,再利用羟基的消去反应引入碳碳双键,将双键与硝基通过加氢最终还原生成氨基,其整个合成路线可表示为:
,再利用羟基的消去反应引入碳碳双键,将双键与硝基通过加氢最终还原生成氨基,其整个合成路线可表示为:
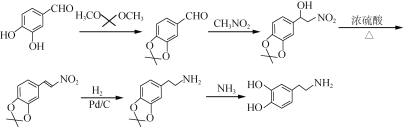 ,
,
故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】对下列图像描述正确的是

A. 图①可表示将氨气通入醋酸溶液至过量过程中溶液导电性的变化
B. 根据图②可判断可逆反应A2(g)+3B2(g)![]() 2AB3(g)的ΔH>0
2AB3(g)的ΔH>0
C. 图③表示等体积、等pH的盐酸与醋酸溶液分别与足量的锌粉发生反应产生氢气的体积(V)随时的变化的示意图
D. 图④可表示压强对可逆反应A(g)+B(g)![]() 2C(g)+D(g)的影响,乙的压强大
2C(g)+D(g)的影响,乙的压强大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界的矿物、岩石的成因和变化受多种条件的影响。地壳内每加深1![]() ,压强增大约25000~30000KPa,温度升高25—30摄氏度。在地壳内SiO2和HF存在以下平衡: SiO2(s)+4HF(g)
,压强增大约25000~30000KPa,温度升高25—30摄氏度。在地壳内SiO2和HF存在以下平衡: SiO2(s)+4HF(g) ![]() SiF4(g)+2H2O(g) + 148.9KJ
SiF4(g)+2H2O(g) + 148.9KJ
根据题意完成下列填空:
(1)该反应的△H________0,在地壳深处容易有____________气体逸出,已知此处温度较高,则该反应为 _____________反应(填“自发”,“非自发”,“无法确定”)
(2)如果上述反应的平衡常数K值变大,该反应__________(填编号)。
A.一定向正反应方向移动
B.正逆反应速率一定加快
C.平衡移动过程为:正反应速率先增大后减小
D.平衡移动过程为:逆反应速率先减小后增大
(3)如果上述反应在体积不变的密闭容器中发生,当反应已经达到平衡时,下列成立的是_______ (填编号)。
a.2 v正(HF) = v逆(H2O) b. v (H2O) = 2v (SiF4)
c. SiO2的质量保持不变 d.反应物不再转化为生成物
(4)若反应容器容积为2.0L,反应时间8.0min,容器内气体的密度增大了0.12g/L,在这段时间内HF的平均反应速率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水FeCl2易吸湿、易被氧化,常作为超高压润滑油的成分。某实验小组利用无水FeCl3和氯苯(无色液体,沸点132.2℃)制备少量无水FeCl2,并测定无水FeCl2的产率。
实验原理:2FeCl3+C6H5Cl![]() 2FeCl2+C6H4Cl2+HCl↑
2FeCl2+C6H4Cl2+HCl↑
实验装置:按如图所示组装好的装置,检查气密性后,向三颈烧瓶A中加入16.76g无水FeCl3和22.5g氯苯。
回答下列问题:

(1)利用工业氮气(含有H2O、O2、CO2)制取纯净干燥的氮气。
①请从下列装置中选择必要的装置,确定其合理的连接顺序:a→________→上图中的j口(按气流方向,用小写字母表示)。

②实验完成后通入氮气的主要目的是________。
(2)装置C中的试剂是________(填试剂名称),其作用是________。
(3)启动搅拌器,在约126℃条件下剧烈搅拌30min,物料变成黑色泥状。加热装置A最好选用__(填字母)。
a.酒精灯 b.水浴锅 c.电磁炉 d.油浴锅
(4)继续升温,在128~139℃条件下加热2h,混合物颜色逐渐变浅,黏度降低。该步骤中加热温度已经接近或超过氯苯沸点,但氯苯实际损失量却非常小,其原因是________。
(5)继续加热1h后放置冷却,在隔绝空气条件下过滤出固体,用洗涤剂多次洗涤所得固体,置于真空中干燥,得到成品。若D中所得溶液恰好与25mL2.0mol·L-1NaOH溶液完全反应,则该实验中FeCl2的产率约为________(保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液。观察到的现象是先出现黄色沉淀,最终出现黑色沉淀。已知有关物质的溶度积Ksp(25 ℃)如下:
AgCl | AgI | Ag2S | |
Ksp(单位省略) | 1.8×10-10 | 1.5×10-16 | 6.3×10-50 |
下列叙述错误的是( )
A. 沉淀转化的实质就是沉淀溶解平衡的移动
B. 溶解度小的沉淀可以转化为溶解度更小的沉淀
C. AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同
D. 25 ℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中有一未知浓度的稀盐酸,某学生在实验室中进行测定盐酸浓度的实验。请完成下列填空:
(1)配制500mL 0.1000mol·L-1 NaOH 标准溶液。
①配制所需的玻璃仪器有:烧杯、量筒、玻璃棒、__________、__________等。
②称取__________g氢氧化钠固体所需仪器有天平(带砝码、镊子)、药匙、__________
(2)取20.00 mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用__________(填仪器名称)盛装配制的标准NaOH溶液进行滴定。重复上述滴定操作23次,记录数据如下:
滴定次数 | 待测盐酸 的体积/mL | 标准NaOH溶液体积 | |
滴定前的刻度/mL | 滴定后的刻度/rnL | ||
第一次 | 20.00 | 0.40 | 20.50 |
第二次 | 20.00 | 4.10 | 24.00 |
第三次 | 20.00 | 1.00 | 24.00 |
(3)①如何判断滴定终点:____________________________。
②根据上述数据,可计算出该盐酸的浓度约为__________mol·L-1。
③排去碱式滴定管中气泡的方法应采用下图操作中的__________(填序号),然后轻轻挤压玻璃球使尖嘴部分充满碱液。

(4)在上述实验中,下列操作(其他操作正确)会造成测定果偏低的有__________(填序号)。
A.酸式滴定管使用前,水洗后未用待测盐酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体中混有Na2CO3固体
D.滴定终点读数时俯视读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA。已知:在无氧条件下,葡萄糖发生反应C6H12O6![]() 2CH3CH2OH+2CO2↑。下列说法正确的是( )
2CH3CH2OH+2CO2↑。下列说法正确的是( )
A. 0.1 mol葡萄糖(C6H12O6)含羟基(—OH)数目为0.6NA
B. 10.0 g质量分数为46%的酒精与足量的钠反应产生氢分子数为0.05NA
C. 常温常压下,4.48 L CO2和NO2的混合气体含原子总数为0.6NA
D. 4.8 g Mg在足量的CO2中完全燃烧,转移电子数目为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素及其化合物广泛存在于自然界中。回答下列问题:
(1)光气(COCl2)是一种重要的有机中间体,在农药、医药、工程塑料、聚氨酯材料以及军事上都有许多用途。光气的分子立体构型为______________,其三种元素的电负性由小到大的顺序为______________。与COCl2互为等电子体的分子和离子(各写一种)__________。
(2)日常生活中,看到的许多可见光,如霓虹灯,试从原子结构角度解释这一现象?____________________________。
(3)区分晶态二氧化硅和非晶态二氧化硅最可靠的科学方法是_____________。
(4)一种铜的溴化物晶胞结构如图所示,若将图中的Cu去掉,再把所有的Br换成Cu,得到晶体铜的晶胞结构,则晶体铜的堆积方式为___________,某同学将基态铜原子价电子错误的写为3d94s2,违背了核外电子排布规律中的______。
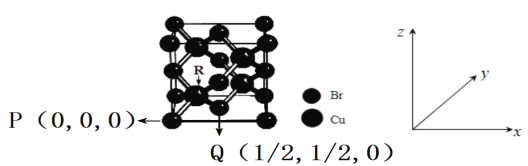
(5)下列关于上述铜的溴化物晶胞结构说法正确的是_________(选填字母序号)。
A.该化合物的化学式为CuBr2
B.铜的配位数为8
C.与每个Br紧邻的Br有12个
D.由图中P点和Q点的原子坐标参数,确定R点的原子坐标参数为(1/4,1/4,1/4)
(6)若图中P点和R点的原子核间距为a cm,NA为阿伏伽德罗常数的值,则该晶胞密度为______g/cm3。(列出计算式即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com