
【题目】氨是重要的化工原料,用途广泛。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+和CH3COO-构成)溶液吸收对氨合成催化剂(铁粉)有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是 。(填元素符号)
②醋酸二氨合铜所含元素的单质,所属的晶体类型有 (填序号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期中,基态原子与基态Cu原子未成对电子数目相同的元素有 种(不包括Cu)。
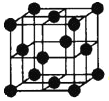
④铜单质为面心立方晶体,其晶胞如图。如果Cu的原子半径为a cm,阿伏加德常数的值为NA,则此种Cu单质的密度表达式为 g/cm3。(相对原子质量Cu:64)

(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3+ NH3=F3B—NH3。写出两种与BF3具有相同空间构型的阴离子 、 。
(3)NH3可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。该物质在水溶液中以SO42-和N4H44+两种正四面体构型的离子存在。N4H44+遇碱生成一种形似白磷的N4分子。画出N4H44+的结构(标明其中的配位键) 。
【答案】(1)① 氮 ② b、c、d③ 4④![]() (2) CO32-、NO3-(3)
(2) CO32-、NO3-(3)
【解析】
试题分析:(1)①非金属性越强,第一电离能越大,但是最外层电子排布处于全满或半满状态时较稳定,不易失电子,第一电离能较大,醋酸二氨合铜所含的元素有Cu、O、C、H、N,由于N原子的最外层排布为半满状态,第一电离能较大,所以第一电离能最大的是氮;
②醋酸二氨合铜所含元素组成的单质,铜属于金属晶体、金刚石属于原子晶体、氧气和氢气属于分子晶体,答案选b、c、d;
③Cu的外围电子排布为3d104s1,只有1个未成对电子,第4周期元素中,基态原子含有一个未成对电子的元素有,K、Sc、Ga、Br,共有4种元素;
④该晶胞中铜原子个数=8×1/8+6×1/2=4,晶胞边长为acm,晶胞体积=(acm)3,密度ρ=(4×M/NA)/V=![]() ;
;
(2)BF3中B的价层电子对数为3+(3-3×1)/2=3,没有孤电子对,分子的空间构型为正三角形,CO32-中碳原子价层电子对个数=3+(4+2-3×2)×1/2=3,且不含孤电子对,所以C原子采用sp2杂化,空间构型为平面三角形,NO3-中N原子形成3个σ键,孤对电子数=(5+13×2)/2,中心原子为sp2杂化,立体构型为平面三角形,所以与BF3具有相同空间构型的阴离子为CO32-;NO3-;
(3)N4H44+中每个N原子与另外3个N原子形成共价键,同时与1个氢离子形成配位键,则N4H44+的结构为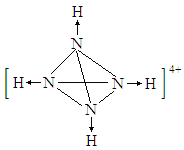 。
。


科目:高中化学 来源: 题型:
【题目】现有下列十种物质,用序号进行填空:
①氢氧化钠 ②铝丝 ③稀硫酸 ④饱和食盐水 ⑤HCl ⑥Na2CO3 ⑦C2H5OH ⑧KCl ⑨CaCO3 ⑩石墨
(1)属于混合物的是________________,属于单质的是________________,属于化合物的是________________。
(2)属于电解质的是________________,既不是电解质又不是非电解质的是________________。
(3)①与⑤反应的离子方程式为________________,②与③反应的离子方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比法是一种重要的化学思维方法。下列各项中的已知和类比结论均正确的是
选项 | 已知 | 类比结论 |
A | 汞可以用热分解法冶炼 | 铜也可以用热分解法冶炼 |
B | Mg-Al插入稀H2SO4溶液中构成 原电池,Mg作负极 | Mg-Al插入稀NaOH溶液中构成原电池,Mg也作负极 |
C | 硫元素的最高正化合价为+6 | 氧元素的最高正化合价也为+6 |
D | Si是半导体材料 | Ge也可作半导体材料 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
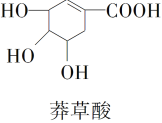
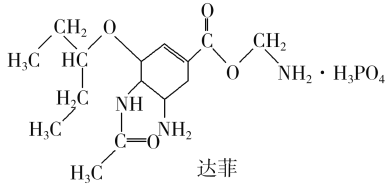
【题目】“达菲”是瑞士罗氏公司研制的有效治疗人类禽流感的药物。达菲的主要合成原料是我国盛产的莽草酸。
下列说法不正确的是( )
A.莽草酸可溶于水
B.1 mol莽草酸最多可和4 molNaOH溶液反应
C.从结构上推测,达菲既可与盐酸反应又可与氢氧化钠溶液反应
D.从结构上推测,以莽草酸为原料合成达菲须经过酯化反应等步骤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁又称聚铁,化学式为[Fe2(OH)n(SO4)3-0.5n]m,广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),过程如下:

(1)验证固体W焙烧后产生的气体含有SO2的方法是:
___________________________________________________________________。
(2)实验室制备、收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器接口,顺序为a→____→____→____→____→f。
装置A中发生反应的化学方程式为_________________________________________。
装置D的作用是_____________,装置E中NaOH溶液的作用是__________________。

(3)制备绿矾时,向溶液X中加入过量__________,充分反应后,经过滤操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾。过滤所需的玻璃仪器有_______________________。
(4)欲测定溶液Y中Fe2+的浓度,需要用容量瓶配制KMnO4标准溶液,定容时视线应_____________________,直到_____________________。用KMnO4标准溶液滴定时应选用________滴定管(填“酸式”或“碱式”)。
(5)溶液Z的pH影响聚铁中铁的质量分数。若溶液Z的pH偏小,将导致聚铁中铁的质量分数______(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)对下列物质进行系统命名:
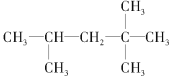 : ;
: ;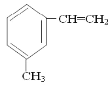 : 。
: 。
(2) ![]() 的分子式为:__________;
的分子式为:__________;
(3)下列几种烃类物质:

①互为同分异构体的有 和 (写名称)。
②正四面体烷的二氯取代产物有______种;立方烷的二氯取代产物有______种。
(4)某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。A的结构简式为 ,名称为_________。A中的碳原子是否都处于同一平面?________(填“是”或“不是”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把0.6 mol X气体和0.6 mol Y气体混合于2 L密闭容器中,使它们发生如下反应:2X(g)+Y(g) == nZ(g)+2W(g) 1 min末已生成0.2 mol W ,若测知以Z的浓度变化表示的反应速率为0.005 mol·L-1·s-1 ,计算:
(1)前1 min内用X的浓度变化表示的平均反应速率。
(2)1 min末时Y的浓度。
(3)化学反应方程式中n的值是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是氢氧燃料电池构造示意图。关于该电池说法正确的是( )。

A.b是负极
B.需要点燃该电池才能开始工作
C.工作时能观察到淡蓝色火焰
D.氢氧燃料电池是一种高效环境友好的发电装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双安妥明是一种降血脂药物,主要用于降低血液中胆固醇浓度,安全,副作用小,其结构简式为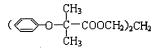 。已知:
。已知:
Ⅰ.![]()
![]()
Ⅱ.![]()
双安妥明的合成路线如下:
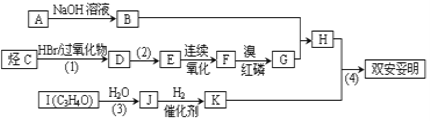
已知:C的分子式为C4H8,且支链有一个甲基;Ⅰ能发生银镜反应且1molI能与2mol氢气发生加成反应;K的结构具有对称性.试回答下列问题:
①写出结构简式:A_________,J _________,C化学名称_________。
②反应(2)的条件是_________,反应(3)的类型是_________。
③写出反应(4)的化学方程式_________。
④与F互为同分异构体,且属于酯类的有机物,写出其中能发生银镜反应的有机物的结构简式_________、_________。
⑤与丙烯酸互为同系物,且相对分子质量为100,其结构共有_________种(不考虑立体异构)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com