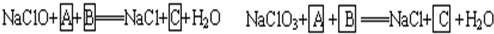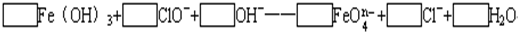(2009?广东模拟)铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁.“速力菲”是市场上一种常见的补铁药物,下表格是它的说明书.

(1)该药品中Fe
2+ 会缓慢氧化,国家规定该药物中Fe
2+ 的氧化率超过10%即不能再服用.
1为了检验某药店出售的“速力菲”是否氧化,实验室可选用最常用最灵敏的检验试剂为
硫氰化钾溶液
硫氰化钾溶液
( 填试剂的名称 )
②实验室采用H
2SO
4酸化的KMnO
4溶液,对“速力菲”中的Fe
2+ 进行滴定(假设药品中,其它成分不与KMnO
4反应).请配平下列离子方程式
1
1
MnO
4-+
5
5
Fe
2++
8
8
H
+═
1
1
Mn
2++
5
5
Fe
3++
4
4
H
2O
③称量上述含铁元素质量分数为20.00% 的“速力菲”10.00g,将其全部溶于稀硫酸中,配制成1000.00mL溶液,取出20.00mL,用0.01mol/L的KMnO
4溶液滴定,用去KMnO
4溶液12.00mL.该药品可以服用吗?
不可以
不可以
(填“可以”或“不可以”),请通过计算简述理由(写出主要计算过程)
由MnO4-~5Fe2+,可得1000.00mL溶液含有的Fe2+的物质的量n(Fe2+)=0.01mol/L×12.00×10-3L×5×(1000.00mL/20.00mL)=0.03mol,m(Fe2+)=0.03mol×56g/mol=1.68g,Fe2+的氧化率(10g×20.00%-1.68g)/(10g×20.00%)=16.00%>10%,所以不可以服用.
由MnO4-~5Fe2+,可得1000.00mL溶液含有的Fe2+的物质的量n(Fe2+)=0.01mol/L×12.00×10-3L×5×(1000.00mL/20.00mL)=0.03mol,m(Fe2+)=0.03mol×56g/mol=1.68g,Fe2+的氧化率(10g×20.00%-1.68g)/(10g×20.00%)=16.00%>10%,所以不可以服用.
.
(2)已知琥珀酸亚铁相对分子质量为172,琥珀酸为有机酸.含23.6g琥珀酸的溶液与4mol/L 100mL的氢氧化钠溶液恰好完全中和.质子核磁共振分析显示,琥珀酸分子中只含有两种位置不同的氢原子.写出琥珀酸溶液与氢氧化钠溶液完全中和的离子方程式(有机物须写结构简式)
HOOC-CH2-CH2-COOH+2OH-→-OOC-CH2-CH2-COO-+2H2O
HOOC-CH2-CH2-COOH+2OH-→-OOC-CH2-CH2-COO-+2H2O
,琥珀酸亚铁的化学式为
FeC4H4O4
FeC4H4O4
.