
����Ŀ����3�������Ϊ4.0 L�ĺ����ܱ������У���Ӧ CO2(g)��C(s)![]() 2CO(g) ��H > 0���ֱ���һ���¶��´ﵽ��ѧƽ��״̬������˵����ȷ����
2CO(g) ��H > 0���ֱ���һ���¶��´ﵽ��ѧƽ��״̬������˵����ȷ����
���� | �¶�/K | ��ʼʱ���ʵ���/mol | ƽ��ʱ���ʵ���/mol | ||
n(CO2) | n(C) | n(CO) | n(CO) | ||
I | 977 | 0.56 | 1.12 | 0 | 0.8 |
II | 977 | 1.12 | 1.12 | 0 | x |
III | 1250 | 0 | 0 | 1.12 | y |
A.977 K���÷�Ӧ�Ļ�ѧƽ�ⳣ��ֵΪ4
B.�ﵽƽ��ʱ��������I������C������ƽ�������ƶ�
C.�ﵽƽ��ʱ������I��CO2��ת���ʱ�����II�еĴ�
D.�ﵽƽ��ʱ������III�е�CO��ת���ʴ���28.6%
���𰸡�C
��������
A������I���Ϊ4L����ʼͶ��Ϊn(CO2)=0.56mol��n(C)=1.12mol��CΪ���壬����Ũ�ȣ�����������ʽ�У�
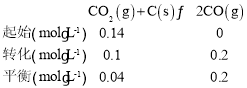
ƽ�ⳣ��K=![]() =1����A����
=1����A����
B��CΪ�����壬��������������C������ƽ�ⲻ�ƶ�����B����
C����II���������ΪI��������Ķ��������I�ﵽ��Чƽ�⣬��������CO2��ת������ͬ����ʵ���ϣ�II���������I���������ȣ�����ѹǿ��������ѹǿƽ�������ƶ������Դﵽƽ��ʱ������II��CO2��ת���ʱ�����I�е�С����C��ȷ��
D��I��������ת������ʼ����ͬ�����¶���ͬ������ߴﵽ��Чƽ�⣬����I��CO2ת����Ϊ![]() =71.4%��������III�е�CO��ת����Ϊ1-71.4%=28.6%����ʵ���������¶ȸ��ߣ��÷�Ӧ����ӦΪ���ȷ�Ӧ���¶�����ƽ�������ƶ�����������CO�ķ����ƶ�������III�е�CO��ת����ҪС��28.6%����D����
=71.4%��������III�е�CO��ת����Ϊ1-71.4%=28.6%����ʵ���������¶ȸ��ߣ��÷�Ӧ����ӦΪ���ȷ�Ӧ���¶�����ƽ�������ƶ�����������CO�ķ����ƶ�������III�е�CO��ת����ҪС��28.6%����D����
�ʴ�ΪC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ�����͵���
A. ����������̿�ʹ��λʱ���ڹ�������ֽ����������������
B. ��ҵ�������ᣬͨ������Ŀ�������߶��������ת����
C. ������ˮpH��С
D. Fe(SCN)3��Һ�м���KSCN����ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1mol��L1��Ԫ����H2A��Һ�м����������ع���ı���Һ��pH����Һ�е�H2A��HA��A2�����ʵ�������![]() (X)��pH�ı仯��ͼ��ʾ[��֪
(X)��pH�ı仯��ͼ��ʾ[��֪![]() (X) =
(X) =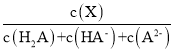 ]�����������������
]�����������������
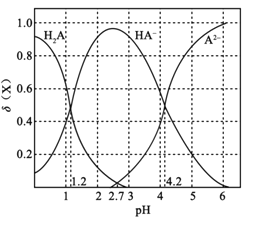
A.pH=1.2ʱ��c(K+)+c(H+)=c(H2A)+c(OH)
B.�����£�H2A�ĵ���ƽ�ⳣ��Ka2=1042
C.pH=2.7ʱ��c(HA)��c(H2A)=c(A2)
D.KHA��Һ������Ũ��Ϊc(K+)��c(HA)��c(OH)��c(H2A)��c(H+)��c(A2)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.����㶼ֻ��2�����ӵ�Ԫ��ԭ������һ������
B.ͬһ����Ԫ���У���һ��������ԭ���������Ӷ�����
C.I3AsF6�����д���I3�����ӣ�I3�����ӵļ��ι���ΪV��
D.H2O2��һ�ֺ��м��Լ��ͷǼ��Լ��ķǼ��Է���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��º��������з�����Ӧ2SO2(g)��O2(g)![]() 2SO3(g)����ʼʱSO2��O2�ֱ�Ϊ20 mol��10 mol���ﵽƽ��ʱ��SO2��ת����Ϊ80%������SO3��ʼ���з�Ӧ������ͬ�������£���ʹƽ��ʱ���ɷֵ����������ǰ����ͬ������ʼʱSO3�����ʵ�����SO3��ת���ʷֱ�Ϊ�� ��
2SO3(g)����ʼʱSO2��O2�ֱ�Ϊ20 mol��10 mol���ﵽƽ��ʱ��SO2��ת����Ϊ80%������SO3��ʼ���з�Ӧ������ͬ�������£���ʹƽ��ʱ���ɷֵ����������ǰ����ͬ������ʼʱSO3�����ʵ�����SO3��ת���ʷֱ�Ϊ�� ��
A. 10mol��10%B. 20mol��20%C. 20mol��40%D. 30mol��80%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᾧ�����ɿɱ�ʾΪH2C2O4��xH2O��Ϊ�˲ⶨxֵ����������ʵ�飺�ٳ�ȡng���ᾧ�����100.00mLˮ��Һ����ȡ25.00 mL�����ƵIJ�����Һ������ƿ�У���ϡ���ᣬ��Ũ��Ϊamol��L��1��KMnO4��Һ�ζ����������ķ�ӦΪ��2KMnO4��5H2C2O4��3H2SO4=K2SO4��10CO2����2MnSO4��8H2O����Ӧ����MnSO4��ˮ��Һ�л�����ɫ���Իش��������⣺
��1��ʵ��̨��������������ʵ���в���Ҫ����___������ţ���
a.������ƽ�������롢���ӣ� b.�ζ��� c.100 mL����ƿ d.�ձ� e.©�� f.��ƿ g.������ h.ҩ�� i.��ƿ
��2��ʵ����KMnO4��ҺӦװ��___ʽ�ζ����У�ԭ����___��
��3���ζ���������ȥVmLamol��L��1��KMnO4��Һ���������ƵIJ�������ʵ���Ũ��Ϊ__mol��L��1���ɴ˿ɼ���x��ֵΪ___��
��4�����ζ��յ����ʱ���ӣ���������xֵ����__����ƫ��ƫС����Ӱ�죩��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڻ�ѧ��Ӧ��˵������ȷ����
A. ͬʱ�ı������������о���Ӧ���ʵı仯���ܸ���ó��йع���
B. ���ȷ�Ӧ�ķ�Ӧ�������Ǵ������ȷ�Ӧ�ķ�Ӧ����
C. һ�������£�ʹ�ô����ܼӿ췴Ӧ���ʲ���߷�Ӧ���ƽ��ת����
D. ��ͬ�¶��£�H2(g)+CO2(g)![]() CO(g)+H2O(g)�У��ܱ����������ַ�Ӧ��Ũ��Ϊ0.020 mol��L-1�ķ�Ӧ���ʴ������ַ�Ӧ��Ũ��Ϊ0.010 mol��L-1�ķ�Ӧ����
CO(g)+H2O(g)�У��ܱ����������ַ�Ӧ��Ũ��Ϊ0.020 mol��L-1�ķ�Ӧ���ʴ������ַ�Ӧ��Ũ��Ϊ0.010 mol��L-1�ķ�Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��д��ȷ����(����)
A. ����Ͷ��NaOH��Һ�У�2Al��2OH��===2AlO2-��H2��
B. Na��CuSO4��Һ��Ӧ��Cu2����2Na===2Na����Cu
C. ��AlCl3��Һ�м��������İ�ˮ��Al3����3OH��===Al(OH)3��
D. Ba(OH)2��Һ��ϡ���ᷴӦ��Ba2����2OH����2H����SO42-===BaSO4����2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2.56gCu��200mLijŨ�ȵ�ŨHNO3��ϣ����ŷ�Ӧ�Ľ��������������ɫ��dz����Cu��Ӧ��ȫʱ�����ռ�������1.12L(��״��)��
���й��ڸ÷�Ӧ�ķ���������ǣ� ��
A.�÷�Ӧ���ɵ�NO2��NO�������Ϊ7 : 3
B.�÷�Ӧת�Ƶ�����Ϊ0.04NA
C.�÷�Ӧ����HNO3�����ʵ���Ϊ0.13mol
D.��Ӧ������������Һ��(���Է�Ӧǰ����Һ����ı仯)c(NO3-) = 0.4 mol��L-1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com