
| A. | ①③⑤⑦ | B. | ③④⑤⑥ | C. | ①②⑤⑦ | D. | ①②⑥⑦ |
科目:高中化学 来源: 题型:选择题
 某溶液中只可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
某溶液中只可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )| A. | 溶液中的阳离子只有H+、Mg2+、Al3+可能含有Fe3+ | |
| B. | 溶液中一定不含CO32-和NO3-,一定含有SO42- | |
| C. | 溶液中c(NH4+)=0.3 mol/L | |
| D. | c(H+):c(Al3+):c(Mg2+)=1:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和乙烯 | B. | 甲烷和丙烯 | C. | 乙烷和乙烯 | D. | 乙烷和丙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度 | |||||
| (×10-3 mol•L-1) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷 | |
| B. | 重结晶法提纯苯甲酸时,为了除去杂质和防止苯甲酸析出,应该趁热过滤 | |
| C. | 配制银氨溶液时,将硝酸银溶液慢慢滴入稀氨水中,产生沉淀后继续滴加到沉淀刚好溶解为止 | |
| D. | 无水乙醇和浓硫酸共热到170℃,将制得的气体通入酸性高锰酸钾可检验制得的气体是否为乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z的浓度为0.4 mol•L-1 | B. | X2、Z的浓度均为0.15 mol•L-1 | ||
| C. | X2与Z的浓度之和为0.4 mol•L-1 | D. | X2的浓度为0.4 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 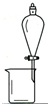 用CCl4提取溴水中的Br2 用CCl4提取溴水中的Br2 | B. | 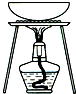 从KI和I2的固体混合物中回收I2 从KI和I2的固体混合物中回收I2 | ||
| C. | 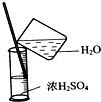 稀释浓硫酸 稀释浓硫酸 | D. | 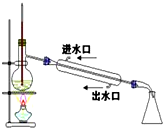 工业酒精制备无水酒精 工业酒精制备无水酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,NaClO属于离子(离子、共价)化合物.
,NaClO属于离子(离子、共价)化合物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com