
| A、①② | B、②③ | C、②④ | D、③④ |


科目:高中化学 来源: 题型:
 将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合溶液中滴加1mol?L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )
将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合溶液中滴加1mol?L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )| A、AB段发生反应的离子方程式为:Ba2++SO42-═BaSO4↓ |
| B、E点对应横坐标稀硫酸的体积为70 mL |
| C、D点表示的沉淀的化学式为Al(OH)3、BaSO4 |
| D、E点沉淀比A点沉淀质量大2.33g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.7g金属铝所含电子数目为0.1 NA |
| B、16 g CH4所含原子数目为NA |
| C、17 g NH3 所含电子数目为NA |
| D、18 g水所含分子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室用NaOH和FeSO4制取Fe(OH)2时,Fe(OH)2很容易被氧化,若采用如图所示装置制取,可以得到较纯净的Fe(OH)2.
实验室用NaOH和FeSO4制取Fe(OH)2时,Fe(OH)2很容易被氧化,若采用如图所示装置制取,可以得到较纯净的Fe(OH)2.查看答案和解析>>
科目:高中化学 来源: 题型:
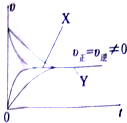 研究碳、氮、硫及其化合物的性质具有重要意义.
研究碳、氮、硫及其化合物的性质具有重要意义.| 活性炭 | NO | E | F | |
| 起始 | 2.500 | 0.500 | 0 | 0 |
| T1 | 2.350 | 0.200 | 0.150 | 0.150 |
| T2 | 2.400 | 0.300 | 0.100 | 0.100 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/L稀硫酸100mL中含有SO42- 个数为0.1NA |
| B、1.7g NH3所含的电子数目为10NA |
| C、2g H2所含原子数目为2NA |
| D、标准状况下,33.6LSO3含有SO3分子数为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、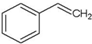 能使溴水褪色,但不能是酸性高锰酸钾溶液褪色 能使溴水褪色,但不能是酸性高锰酸钾溶液褪色 |
| B、乙烯能和溴水、酸性高锰酸钾溶液发生加成反应使之褪色 |
| C、气态烃CxHy与适量O2恰好完全反应,如果反应前后气体体积不变(温度>100℃),则 y=4 |
| D、相同质量的烃,完全燃烧,消耗O2越多,烃中含碳的质量分数越高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯和浓溴水用铁做催化剂制溴苯 |
| B、将苯与浓硝酸混合共热制硝基苯 |
| C、甲烷与氯气光照制得纯净的一氯甲烷 |
| D、乙烯通入溴的四氯化碳溶液得到1,2-二溴乙烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com