
【题目】向100mL 1.0molL﹣1的AlCl3溶液中逐滴加入0.5molL﹣1的NaOH溶液至过量,生成沉淀的物质的量与加入NaOH的量的理论曲线图正确的是( )
A.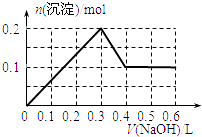
B.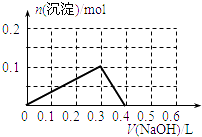
C.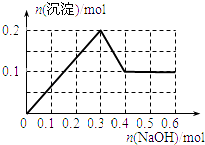
D.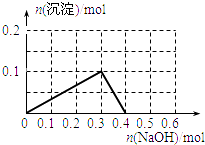
【答案】D
【解析】解:向氯化铝溶液中加入氢氧化钠溶液发生的化学反应为:AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3+NaOH=NaAlO2+2H2O,当铝离子恰好和氢氧化钠完全反应生成氢氧化铝时,沉淀的物质的量最大,当氢氧化铝完全转化为偏铝酸钠时,沉淀完全消失;
根据方程式AlCl3+3NaOH=Al(OH)3↓+3NaCl、Al(OH)3+NaOH=NaAlO2+2H2O知,铝离子完全转化为沉淀和沉淀完全消失需要氢氧化钠的物质的量之比为3:1,n(AlCl3)=1.0mol/L×0.1L=0.1mol,完全沉淀时需要氢氧化钠溶液的体积= ![]() =600mL,根据原子守恒得n(Al(OH)3)=n(AlCl3)=0.1mol,
=600mL,根据原子守恒得n(Al(OH)3)=n(AlCl3)=0.1mol,
故选D.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】实验室里通常用MnO2与浓盐酸反应制取氯气,为进行有关氯气的性质实验,需要4瓶容积为100mL的氯气.(常温下,氯气的密度为2.91g/L)
(1)写出制取氯气的离子方程式.
(2)制取4瓶氯气,理论上需要MnO2固体的质量是多少?
(3)制取4瓶氯气,被氧化的HCl的物质的量是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用少量的溴水和足量的乙醇制备1,2﹣二溴乙烷的装置如下图所示: 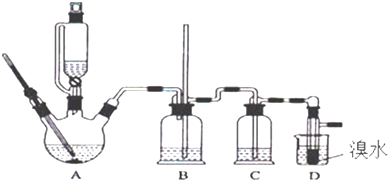
有关数据列表如下:
乙醇 | 1,2﹣二溴乙烷 | 醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | ﹣l30 | 9 | ﹣1l6 |
回答下列问题:
(1)烧瓶A中发生的主要的反应方程式 .
(2)装置B的作用是 .
(3)在装置C中应加入(填字母). a.水 b.浓硫酸 c.饱和碳酸氢钠溶液 d.氢氧化钠溶液
(4)若产物中有少量未反应的Br2 , 最好用(填字母)洗涤除去. a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇 e.Na2SO3溶液
(5)若产物中有少量副产物乙醚,可用的方法除去.
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是 .
(7)判断该制备反应已经结束的最简单方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鉴别食盐水和蔗糖水的方法有:①在两种溶液中分别加入少量稀硫酸,加热,再加入碱中和硫酸,再加入银氨溶液,微热;②测量溶液的导电性;③将溶液与溴水混合、振荡;④用舌头尝味道。其中在实验室进行鉴别的正确方法是( )
A.①②
B.①③
C.②③
D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是( )
A.淀粉和油脂的水解都是高分子生成小分子的过程
B.2﹣甲基丙烷和异丁烷互为同系物
C.![]() 属于取代反应
属于取代反应
D.C3H4Cl2的链状有机物的同分异构体有5种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某待测溶液中只可能含有Ag+、Fe2+、Na+、Ba2+、 ![]() 、
、 ![]() 、
、 ![]() 中的几种离子,依次进行下列实验: ①取少量待测液,加入足量的NaCl溶液,没有明显现象
中的几种离子,依次进行下列实验: ①取少量待测液,加入足量的NaCl溶液,没有明显现象
②继续加入足量的Na2SO4溶液,有白色沉淀生成
③过滤,取少量滤液,加入足量的NaOH溶液,有白色絮状沉淀生成,迅速变为灰绿色,最后变为红褐色
根据实验现象回答:
(1)待测液中一定含有离子,一定没有离子.
(2)写出步骤②中发生反应的离子方程式 .
(3)写出步骤③中沉淀由白色变为红褐色的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于苯乙烯(结构如图)的下列叙述中:①能使酸性KMnO4溶液褪色;②可发生加聚反应;③可溶于水;④可溶于苯中;⑤能与浓硝酸发生取代反应;⑥所有的原子可能共平面,其中正确的是( ) ![]()
A.仅①②④⑤
B.仅①②⑤⑥
C.仅①②④⑤⑥
D.全部正确
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com