
| A. | 一样多 | B. | 后者较前者多 | C. | 前者较后者多 | D. | 无法比较 |
科目:高中化学 来源: 题型:选择题
| A. | 生成2molSO3 | |
| B. | SO2和SO3物质的量之和一定为2mol | |
| C. | 放出197kJ的热量 | |
| D. | 平衡时容器内气体压强和开始时压强相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )合成聚芳酯E的路线:
)合成聚芳酯E的路线:
 +SOCl2→
+SOCl2→ +SO2+HCl
+SO2+HCl +R′OH→
+R′OH→ +HCl (R、R′表示烃基)
+HCl (R、R′表示烃基) .
. .
. 结构
结构 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 蒸馏操作时,应使温度计水银球置于混合液中 | |
| B. | 蒸馏操作时,冷却水应从冷凝管的下口通入,上口流出 | |
| C. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| D. | 蒸发操作时,应使混合物中的水分完全蒸干后,再停止加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
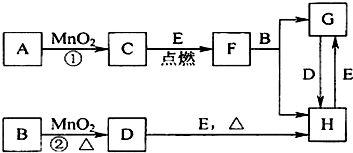
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com