
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 充分吸收了Na2SiO3饱和溶液的小木条,沥干后放在酒精灯外焰加热 | 小木条不燃烧 | Na2SiO3可能防火剂 |
| B | 将H2在充满Cl2的集气瓶中燃烧 | 集气瓶口上方有白烟生成 | H2、Cl2化合生成HCl |
| C | 将SO2通入酸性高锰酸钾溶液中 | 溶液褪色 | SO2具有漂白性 |
| D | 除去表面氧化膜的铝箔,在酒精灯上充分加热 | 铝不能滴落下来 | 铝熔点高,没能熔化 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.小木条不燃烧,证明硅酸钠能够防火,可作木材的防火剂;
B.集气瓶口上方有白雾生成,不是白烟;
C.该反应中二氧化硫被酸性高锰酸钾溶液氧化,二氧化硫表现了还原性;
D.铝与氧气反应生成氧化铝的熔点高,导致铝箔在酒精灯火焰上加热熔化但不滴落.
解答 解:A.充分吸收了Na2SiO3饱和溶液的小木条,沥干后放在酒精灯外焰加热,小木条不燃烧,证明Na2SiO3不燃烧,可作防火剂,故A正确;
B.将H2在充满Cl2的集气瓶中燃烧生成氯化氢,氯化氢极易溶于水,在集气瓶口上方形成盐酸小液滴,则有白雾生成,故B错误;
C.将SO2通入酸性高锰酸钾溶液中,溶液褪色,二氧化硫被氧化,表现了是还原性,不是漂白性,故C错误;
D.金属Al与氧气反应生成氧化铝的熔点高,则铝箔在酒精灯火焰上加热熔化但不滴落,不是铝的熔点高,故D错误;
故选A.
点评 本题考查了化学实验方案的评价,题目难度中等,涉及硅酸钠、二氧化硫、铝及氧化铝的性质等知识,明确常见元素及其化合物性质即可解答,试题培养了学生的灵活应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 加入硝酸银溶液产生白色沉淀,一定有Cl- | |
| B. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ | |
| D. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在100 g质量分数为30%的甲醛水溶液中,含有氢原子数为2NA | |
| B. | 7.8 g Na2S和Na2O2固体混合物中,含有的阴离子数为0.1NA | |
| C. | 1mol乙醇含有共价键的总数7NA | |
| D. | 反应2SO2(g)+O2(g)?2 SO3 (g),单位时间内消耗NA个O2分子的同时生成2NA个SO3分子,此时反应达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9 g超重水(3H216O)含中子数为6NA | |
| B. | 标准状况下,22.4 L CCl4含有的分子数目为NA | |
| C. | 常温常压下,16g甲烷中共价键数目为4NA | |
| D. | 1 L 0.1 mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11g CO2含有的共用电子对数为0.5NA | |
| B. | 1mol Na分别与足量的O2反应生成Na2O或Na2O2,失去的电子数均为NA | |
| C. | 通常状况下,39 g Na2O2固体中含有的离子总数为2NA | |
| D. | 滴加到沸水中的FeCl3溶液有5.6 g Fe3+发生水解,则生成的胶粒数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 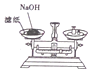 称取一定量的NaOH | |
| B. | 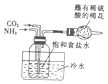 制取NaHCO3 | |
| C. | 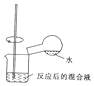 检验浓硫酸与铜反应后的产物中是否含有铜离子 | |
| D. | 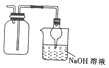 收集NO2丙防止其污染环境 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用大理石和稀盐酸制取CO2:2H++CO32-═CO2↑+H2O | |
| B. | 铁和稀硫酸反应:Fe+2H+═H2↑+Fe3+ | |
| C. | 向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | NaHCO3溶液与NaOH溶液反应:OH-+HCO3-═CO32-+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com