
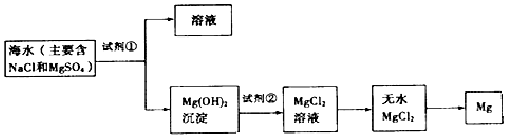
���� �������й�ҵ����ͼ��֪����ˮ�м���ʹþ���ӳ��������˵õ�������þ��������þ����������Ȼ�þ��Һ���Ȼ�þ��Һ����������������Ũ������ȴ�ᾧ������ϴ�ӵõ��Ȼ�þ���壬���Ȼ��������м��ȵ���ˮ�Ȼ�þ��������ڵ��Ȼ�þ�ɵ�þ��
��1�����ԱȽ������۵���ŵ��ȱ�㣬�ۺϷ�����
��2�����Ȼ�þת��Ϊ������þ�ķ����Լ�ԭ�ϵijɱ���˼����Ϊ��ʹþ���ӳ���������������õ��صı��ǣ���Ҫ�ɷ�Ϊ̼��ƣ���Դ��ó�������������Լ������������ƣ�������ȡ�Լ�����̼��Ƹ��·ֽ����������ƺͶ�����̼������������ˮ�����������ƣ�
��3������������Һ�ķ���Ϊ���ˣ�
��4��������þת��Ϊ�Ȼ�þ����Ҫ�������ᷴӦ���Ȼ�þˮ���ᄃ��������HCl�����м��Ȼ����ˮMgCl2���������Ȼ�þˮ������������þ��
��5����ҵ����ȡ����þ�ķ����ǵ�������Ȼ�þ��
��� �⣺��1��ѧ�����������۵���ȣ���ˮ��þ����Ũ��С��ʹ�õij����������ϴ��Ҳ������ռ�������þ�����ѧ���Ĺ۵㲻��ȷ��ԭ���ǣ���ˮ��þ����Ũ��С��������������������þ���ӵij�����
ѧ������ѧ������ȣ�����ɹ�κ�Ŀ�±����Լ��Դ���ɱ��ͣ���ѧ�������þ����Ũ�ȸߣ�������þԪ�صĸ��������ѧ���ҵĹ۵���ȷ����Ϊ��þ���Ӹ���Ũ�ȸߣ��ɱ��ͣ�
ѧ�����������۵���ȣ�����������ˮ�����ĵ���Դ�࣬�ɱ�̫�ߣ����ѧ�����Ĺ۵㲻��ȷ��ԭ���ǣ���Դ���Ĵ�ˮ���ۺ����õͣ��ɱ��ߣ�
�ʴ�Ϊ���ң�
��2����̼��Ƹ��·ֽ�õ������ƣ���������ˮ��Ӧ�����������ƣ��������������Ȼ�þ��Ӧ����������þ��������Լ�����Ca��OH��2���ɱ�����ȡ�Լ��ٵ���ػ�ѧ����ʽ��CaCO3 $\frac{\underline{\;����\;}}{\;}$CaO+CO2���� CaO+H2O�TCa��OH��2��
�ʴ�Ϊ��Ca��OH��2�� CaCO3 $\frac{\underline{\;����\;}}{\;}$CaO+CO2���� CaO+H2O�TCa��OH��2��
��3�������Լ��ٺ��ܹ�����õ�Mg��OH��2�����ķ����ǹ��˷��������ѡD��
�ʴ�Ϊ��D��
��4��Ҫʹ������þת��Ϊ�Ȼ�þ������Ҫ�������ᷴӦ�����Լ��������ᣬ��ҵ�����г����������ᾧ����Ȼ�þˮ���ᄃ��������HCl�����м��Ȼ����ˮMgCl2����Ŀ��������ˮ�⣬�õ���������ˮ�Ȼ�þ��
�ʴ�Ϊ��HCl������ˮ�⣬�õ���������ˮ�Ȼ�þ��
��5����ҵ��ȡþʱ���������״̬���Ȼ�þ��MgCl2$\frac{\underline{\;ͨ��\;}}{\;}$Mg+Cl2����
�ʴ�Ϊ����MgCl2$\frac{\underline{\;ͨ��\;}}{\;}$Mg+Cl2����
���� ���������ת������ѧ��Ӧ�����������ӡ���ˮ��ȡþ�Ĺ��̵��������жϣ�ͨ������Ҫѧ���������۲�ͬ���������ӣ��Ӷ�ѡ�����ѷ�������ҵ���̵�ԭ����ʵ���������Ŀ�Ѷ��еȣ�


 ����С״Ԫ��������������ϵ�д�
����С״Ԫ��������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ʒ��ʴʱ�ȿ�������Ҳ�������� | |
| B�� | ����Ʒ��ʴʱ���缫������ӦΪ��Fe-3e-=Fe2+ | |
| C�� | ����Ʒ��ʴʱ�������ⸯʴ����������ʴ | |
| D�� | ����Ʒ���ӵ�Դ�����ɷ�ֹ��ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���е�һ�֣���
���е�һ�֣����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ù�����ˮ���չ�ҵβ���е�SO2��NH3•H2O+SO2�TNH4++HSO3- | |
| B�� | �Ȼ��ƹ�����Ũ�����ϼ��ȣ�2H++H2SO4+2Cl-$\frac{\underline{\;��\;}}{\;}$SO2��+Cl2��+2H2O | |
| C�� | ������������ϡ���3 Fe2++4H++NO3-�T3Fe3++NO��+2H2O | |
| D�� | 0.01 mol•L-1 NH4Al��SO4��2��Һ��0.02 mol•L-1Ba��OH��2��Һ�������ϣ�NH4++Al3++2SO42-+2Ba2++4OH-�T2BaSO4��+Al��OH��3��+NH3•H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com