
已知五种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.104 | 0.111 | 0.066 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
下列叙述正确的是( )
A.L与T形成的化合物属于共价化合物 B.M的最高价氧化物的水化物具有两性
C.T、Q的氢化物常温常压下均为无色气体 D.L、M的单质与稀盐酸反应速率:M>L
科目:高中化学 来源: 题型:
恒温恒容条件下,能使A(g)+B(g)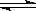 C(g)+D(s)正反应速率加快的是
C(g)+D(s)正反应速率加快的是
A.减少C或D的物质的量
B.体积不变充入氦气使压强增大
C.减少B的物质的量
D.增大A或B的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃,水的电离达到平衡: H2O H++OH-;H>0,下列叙述正确的是
H++OH-;H>0,下列叙述正确的是
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,KW增大,pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一: 甲同学研究的实验报告如下表:
| 实 验 步 骤 | 现 象 | 结 论 |
| ①分别取等体积的2 mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg。 | 反应快慢: Mg>Fe>Cu | 反应物的性质越活泼,反应速率越快。 |
该同学的实验目的是研究_____________对反应速率的影响;根据控制变量法,要得出正确的实验结论,还需控制的实验条件是保持__________相同。
实验二:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1) 针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想反应速率明显加快的原因还可能是_________ _。
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还需要选择的试剂最合理的是 (选填编号)。
A.硫酸钾 B.硫酸锰 C.水 D.氯化锰
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化中,吸收的热量用于克服分子间作用力的是( )
A.液氨受热蒸发 B.加热碘化氢气体使之分解
C.加热氯化钠晶体使之熔化 D.HCl气体溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是 ( )
A.双原子单质分子中的共价健一定是非极性键
B.在共价化合物中一定含有共价键
C.含有离子键的化合物一定是离子化合物
D.含有共价键的化合物一定是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
将10molH2和5molN2放入容积为10L的密闭容器中,某温度下发生反应:3 H2 (g)+N2 (g)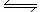 2NH3(g),在最初2s内,消耗H2的平均速率为0.06mol·L-1·s-1,则在这段时间内,用氨气表示的反应速率v(NH3)= __ mol·L-1·s-1 ; 2s时,容器中有________mol H2,此时NH3的物质的量浓度为______ mol·L-1·s-1;推测1s时n(NH3) 0.4moL(填“<”、“>”或“=”)
2NH3(g),在最初2s内,消耗H2的平均速率为0.06mol·L-1·s-1,则在这段时间内,用氨气表示的反应速率v(NH3)= __ mol·L-1·s-1 ; 2s时,容器中有________mol H2,此时NH3的物质的量浓度为______ mol·L-1·s-1;推测1s时n(NH3) 0.4moL(填“<”、“>”或“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com