
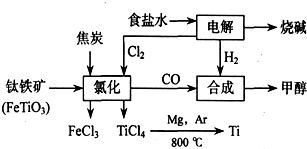
���� ��ͼ��֪����ⱥ��ʳ��ˮ����NaOH��������������������CO�ϳɼ״���������C����������������ԭ��Ӧ��Mg��ԭTiCl4�õ�Ti��
��1�����ʳ��ˮ����NaOH��H2��Cl2���Դ���д���ӷ���ʽ��
��2����ͼʾ��֪�Ȼ�ʱ�ķ�Ӧ��ΪFeTiO3��C��Cl2��������ΪFeCl3��TiCl4��CO���ٸ��ݵ�ʧ���Ӻ�ԭ���غ㼴�ɵó��÷�Ӧ�ķ���ʽ��
��3��A��1mol��ȼ��ȼ�������ȶ�������ų�������Ϊȼ���ȣ�
B����Ӧ��Ϊ��Ӧ�����������������������IJ�ֵ��
C�����ʵ����뷴Ӧ�ų������������ȣ�
D����ͼ��֪��ת�������д����ж�����IJ��룮
��4������CO+2H2��CH3OH��2FeTiO3+6C+7Cl2$\frac{\underline{\;����\;}}{\;}$2TiCl4+2FeCl3+6CO��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH-+H2��+Cl2����֪CH3OH��CO��$\frac{7}{6}$Cl2��$\frac{7}{6}$H2���Դ˼��㣻
��5�����Լ״�����У��״��ڸ�����ʧ���ӷ���������Ӧ��
��� �⣺��ͼ��֪����ⱥ��ʳ��ˮ����NaOH��������������������CO�ϳɼ״���������C����������������ԭ��Ӧ��Mg��ԭTiCl4�õ�Ti��
��1�����ʳ��ˮ����NaOH��H2��Cl2����Ӧ�����ӷ���ʽΪ2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH-+H2��+Cl2����
�ʴ�Ϊ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH-+H2��+Cl2����
��2����ͼʾ��֪�Ȼ�ʱ�ķ�Ӧ��ΪFeTiO3��C��Cl2��������ΪFeCl3��TiCl4��CO���ٸ��ݵ�ʧ���Ӻ�ԭ���غ㼴�ɵó��÷�Ӧ�ķ���ʽΪ2FeTiO3+6C+7Cl2$\frac{\underline{\;����\;}}{\;}$2TiCl4+2FeCl3+6CO��
�ʴ�Ϊ��2FeTiO3+6C+7Cl2$\frac{\underline{\;����\;}}{\;}$2TiCl4+2FeCl3+6CO��
��3��A��Mg������O2��ȼ�գ���641kJ/mol���ܳ���ȼ���ȣ���A����
B����ӦTi��s��+2Cl2��g��=TiCl4��s��Ϊ���ȷ�Ӧ��1mol Ti��s����2mol Cl2 ��g��������������1mol TiCl4 ��s��������������B����
C������������Ϊ24g����Mg��s��������Cl2��g����Ӧ�ų�641kJ������24gTi��s�� ������Cl2��g����Ӧ�ų�������=$\frac{24g}{48g/mol}$��770kJ=385kJ����C��ȷ��
D����ұ��Ti����������CO�Ⱦ�����Ⱦ�����������϶Ի����Ѻã���D����
�ʴ�Ϊ��C��
��4������CO+2H2��CH3OH��2FeTiO3+6C+7Cl2$\frac{\underline{\;����\;}}{\;}$2TiCl4+2FeCl3+6CO��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH-+H2��+Cl2����֪CH3OH��CO��$\frac{7}{6}$Cl2��$\frac{7}{6}$H2����������1 molCH3OH�������ϻ��貹��������2-$\frac{7}{6}$��mol=$\frac{5}{6}$mol����$\frac{5}{3}$gH2��������192 t CH3OH���貹��H2������Ϊ$\frac{192}{32}$��$\frac{5}{3}$=10t��
�ʴ�Ϊ��10��
��5�����Լ״�����У������ϼ״�ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ���缫��ӦʽΪCH3OH-6e-+8OH-=CO32-+6H2O��
�ʴ�Ϊ��CH3OH-6e-+8OH-=CO32-+6H2O��
���� ���⿼���Ϊ�ۺϣ����������Ʊ��������ᴿ���ۺϿ��飬Ϊ��Ƶ���㣬�漰���ӷ���ʽ����ѧ��Ӧ���������绯ѧ��֪ʶ����Ŀ�Ѷ��еȣ���4���й�ϵʽ������Ϊ�����ѵ㣮


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
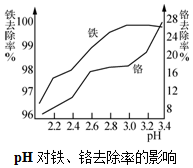 ��ʽ�����������Ƥ�ӡȾ����ҵ��
��ʽ�����������Ƥ�ӡȾ����ҵ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
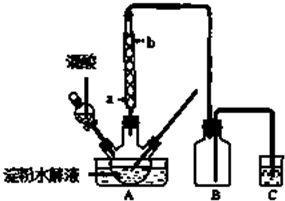
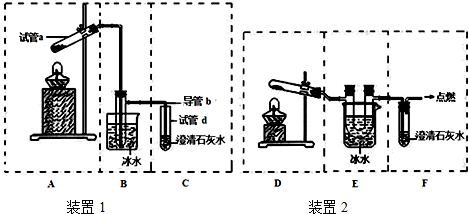
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯī������ʯ�ȶ� | |
| B�� | ���ʯ����ʯī�ȶ� | |
| C�� | ����ú�������ȼ�Ϻ�ȼ��Ч�ʱ�� | |
| D�� | �������Ľ��ʯ��ʯī��ȫȼ�գ�ʯī�ų��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼������ȷֽ� | B�� | �������������Ʒ�Ӧ | ||
| C�� | ����ȼ�� | D�� | ���������ᷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Ʊ�����ú���� | |
| B�� | ����ᱣ��������ƿ�� | |
| C�� | ���Ƶ���ˮ��������ɫ����ƿ�� | |
| D�� | ����������Һ�����ھ߲������IJ���ƿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �ⶨʱ��/h | 0 | 1 | 2 | 3 | 4 |
| ��ˮ��Ʒ��pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com