
| A. | 在NaHS溶液中滴入少量的CuCl2溶液产生黑色沉淀,HS-电离程度增大,反应后溶液pH减小 | |
| B. | 浑浊的苯酚试液中加入饱和Na2CO3溶液变澄清,则酸性:苯酚>碳酸 | |
| C. | 在等浓度NaCl和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl,则Ksp(AgCl)<Ksp(Ag2CrO4) | |
| D. | 等体积、物质的量浓度的HA与NaA(HA为弱酸)混合溶液,其酸碱性取决于Ka(HA)的大小 |
分析 A、HS-电离出的S2-与Cu2+结合生成CuS沉淀;
B、苯酚和碳酸钠反应生成可溶性的碳酸氢钠和苯酚钠;
C、在等浓度NaCl和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl,说明Cl-和CrO42-沉淀时,所需的c(Cl-)更小;
D、Ka(HA)越大,酸性越强;
解答 解:A、在NaHS溶液中,滴入少量CuCl2溶液,HS-电离出的S2-与Cu2+结合生成CuS沉淀,HS-电离程度增大,pH减小,故A正确;
B、C6H5OH+Na2CO3→C6H5ONa+NaHCO3,苯酚钠和碳酸氢钠都是易溶性物质,所以溶液变澄清,说明酸性苯酚>碳酸氢根离子,故B错误;
C、在等浓度NaCl和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl,说明Cl-和CrO42-沉淀时,所需的c(Cl-)更小,但由于AgCl和Ag2CrO4的Ksp表达式不同,故不能说明Ksp(AgCl)<Ksp(Ag2CrO4),故C错误;
D、Ka(HA)越大,酸性越强,如HA电离程度大于A-水解程度,则溶液呈酸性,否则呈碱性,故D正确.
故选AD.
点评 本题考查电离平衡的移动比较,溶解平衡常数的计算,应注意的是混合液显酸碱性的取决因素,题目难度中等,属于易错题.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
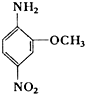 2-氨基-5-硝基苯甲醚俗称红色基B,其结构简式如右所示.若化学式与红色基B相同,且氨基与硝基直接连在苯环上并呈对位时的同分异构体数目(不包括红色基B)可能为( )
2-氨基-5-硝基苯甲醚俗称红色基B,其结构简式如右所示.若化学式与红色基B相同,且氨基与硝基直接连在苯环上并呈对位时的同分异构体数目(不包括红色基B)可能为( )| A. | 6种 | B. | 7种 | C. | 9种 | D. | 10种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 草酸亚铁晶体(FeC2O4•2H2O)呈淡黄色.某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究.
草酸亚铁晶体(FeC2O4•2H2O)呈淡黄色.某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究.| 实验步骤(不要求写出具体操作过程) | 预期实验现象和结论 |
| 取少量黑色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合溶液中由水电离出来的c(OH-)=1×10-9mol/L | |
| B. | c(OH-)-c(HY)=c(H+)=1×10-5mol/L | |
| C. | 混合溶液中c(Na+)=c(Y-)+c(HY)=0.15mol/L | |
| D. | 混合溶液中离子浓度大小次序为:c(Y-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氟元素的非金属性最强,所以氢氟酸的酸性最强 | |
| B. | 元素的金属性越强,其最外层电子数就越少 | |
| C. | 在天然元素中,都含有同位素 | |
| D. | 某元素的原子及其阴离子的核外电子层数等于该元素所在的周期数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com