
| 元素 | 相关信息 |
| X | X的原子L层电子数是K层电子数的2倍 |
| Y | Y是短周期元素中原子半径最大的元素(除稀有气体元素外) |
| Z | Z的原子最外层电子数等于电子层数 |
| W | W原子最外层电子数是X、Z原子最外层电子数之和 |
 ,X的气态氢化物电子式为
,X的气态氢化物电子式为 .
.
分析 X:元素原子L层电子数是K层电子数的2倍,则核外电子排布为1s22s22p2,为C元素;Y:电子层越大,半径越大,同周期,从左向右原子半径减小,则Na是短周期元素中原子半径最大的主族元素;X、Y、Z、W均是周期表中短周期元素,原子序数逐渐增大,Z处于第三周期,Z元素原子的最外层电子数等于电子层数,则Z为Al,W处于第三周期,原子最外层电子数是X、Z原子最外层电子数之和为4+3=7,为氯元素.
(1)X的最高价氧化物为二氧化碳,二氧化碳为直线型结构,分子中存在两个碳氧双键,X的气态氢化物为甲烷,根据1个甲烷分子中含1个C、4个H原子,为正四面体,碳原子最外层有4个电子,能形成4个共价键达到稳定结构,每个氢原子能形成一个共价键达到稳定结构;
(2)根据电子层数等于周期数,最外层电子数等于族序数分析;YW为氯化钠,氯化钠是离子化合物,用电子式表示其形成过程时,左边是原子的电子式,右边为氯化钠的电子式,中间用箭头连接;
(3)①过量的二氧化碳与氢氧化钠反应生成碳酸氢钠;
②铝和氢氧化钠溶液反应生成偏氯酸钠和氢气;
③氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水.
解答 解:(1)X的核外电子排布为1s22s22p2,X的最高正价是+4价,为C元素,最高价氧化物为二氧化碳,二氧化碳为直线型结构,分子中存在两个碳氧双键,二氧化碳的电子式为: ;X的气态氢化物为甲烷,1个甲烷分子中含1个C、4个H原子,分子式为CH4,碳原子的最外层有4个电子,氢原子最外层1个电子,一个碳原子形成4对共用电子对,一个氢原子形成一对共用电子对,所以电子式为:
;X的气态氢化物为甲烷,1个甲烷分子中含1个C、4个H原子,分子式为CH4,碳原子的最外层有4个电子,氢原子最外层1个电子,一个碳原子形成4对共用电子对,一个氢原子形成一对共用电子对,所以电子式为: ,
,
故答案为:+4; ;
; ;
;
(2)W处于第三周期,原子最外层电子数是X、Z原子最外层电子数之和为4+3=7,为氯元素,氯原子结构示意图是 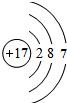 ,属于第三周期第ⅦA族,YW为氯化钠,NaCl为离子化合物,书写电子式时注意,左边写钠原子和氯原子电子式,右边写氯化钠的电子式,中间用箭头连接,形成过程为:
,属于第三周期第ⅦA族,YW为氯化钠,NaCl为离子化合物,书写电子式时注意,左边写钠原子和氯原子电子式,右边写氯化钠的电子式,中间用箭头连接,形成过程为: ,
,
故答案为:第三周期第ⅦA族; .
.
(3)Y:电子层越大,半径越大,同周期,从左向右原子半径减小,则Na是短周期元素中原子半径最大的主族元素,其最高价氧化物对应水化物为氢氧化钠,
①过量的二氧化碳与氢氧化钠反应生成碳酸氢钠,化学反应方程式为:CO2+NaOH═NaHCO3,该离子反应为:CO2+OH-=HCO3-,
故答案为:CO2+OH-=HCO3-;
②X、Y、Z、W均是周期表中短周期元素,原子序数逐渐增大,Z处于第三周期,Z元素原子的最外层电子数等于电子层数,则Z为Al,铝与NaOH溶液反应生成偏铝酸钠和氢气,化学反应为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,离子反应为:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
③氯气和氢氧化钠溶液反应,生成氯化钠、次氯酸钠和水,离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O.
点评 本题考查原子结构与元素周期律,侧重于学生的分析能力的考查,为高考常见题型,根据相关信息推断元素是解题关键,注意掌握元素周期律,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 原电池的电极材料中必须至少有一极是金属 | |
| C. | 牺牲阳极的阴极保护法是利用了电解原理 | |
| D. | 用电解法精炼铜时,粗铜作阳极,纯铜作阴极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应开始时的速率:甲=乙 | |
| B. | 反应所需时间:甲<乙 | |
| C. | 反应开始时,酸的物质的量浓度:乙<甲 | |
| D. | 反应结完后溶液的pH值:甲<乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含有分子数相同 | B. | 所含有氧原子的个数相等 | ||
| C. | 所含有氢原子的个数不相等 | D. | 所含有原子的总数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 项目 | 结论 |
| A | 三种有机化合物:丙烯、氯乙烯、苯 | 分子内所有原子均在同一平面 |
| B | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 | 属于同一反应类型 |
| C | 乙烯和苯都能使溴水褪色 | 褪色的原理相同 |
| D | C5H10O2属于羧酸的同分异构体数目 | 共有4种 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2的排放是形成酸雨的主要原因 | |
| B. | SO2能使酸性高锰酸钾褪色是因为SO2具有漂白性 | |
| C. | 实验室制备少量SO2可以用Na2SO3和浓硫酸加热制备 | |
| D. | SO2的收集应采用向上排空气法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com