
| A、只能与酸反应 |
| B、医疗上可用于治疗胃酸过多 |
| C、与足量的酸反应时放出的CO2比与等质量的Na2CO3要少 |
| D、同温度时,NaHCO3的溶解度>Na2CO3溶解度 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
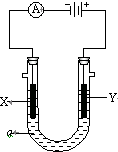 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有②③ | B、只有①② |
| C、只有①③ | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| A | 所有单质中密度最小 |
| B | 形成化合物种类最多的元素 |
| D | 基态原子中只有3个能级,有2个未成对电子 |
| E | 短周期中原子半径最大 |
| F | 第三周期中电负性最大的元素 |
| G | 最外层只有一个电子,内层填满电子 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3COOH |
| B、H2SO4 |
| C、NaOH |
| D、Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 下表是元素周期表前三周期的一部分,按要求作答:
下表是元素周期表前三周期的一部分,按要求作答: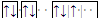

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:W>Z>Y>X |
| B、Y元素在周期表中的位置为第三周期第ⅣA族 |
| C、1 mol甲与足量的乙完全反应共转移了1 mol电子 |
| D、1.0 L 0.1 mol?L-1戊溶液中阴离子总的物质的量小于0.1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2气体缓慢通入Na2O2粉末中:2Na2O2+2SO2=2Na2SO3+O2 |
| B、Fe(NO3)2浓溶液中通入HCl气体:Fe2++2H++NO3-=Fe3++NO2↑+H2O |
| C、碳酸镁溶于硝酸中:CO32-+2H+=CO2↑+H2O |
| D、Mg(HCO3)2溶液中加入过量的苛性钾溶液:Mg2++HCO3-+3OH-=Mg(OH)2+CO32-+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com