
X、Y、Z、W、T是原子序数依次増大的五种短周期元素,且X、Y、Z、W的原子序数之和为32。其中X是元素周期表中原子半径最小的元素,Y、Z左右相邻,Z、W位于同一主族。T的单质常用于自来水的杀菌消毒。
请回答下列问题:
(1)W元素在周期表中的位置为:____________________
(2)由 X、Y、Z、W四种元素中的三种组成一种强酸,该强酸的稀溶液能与金属铜反应,该反应的离子方程式为____________________。
(3)Y元素的气态氢化物与其最高价氧化物的水化物可以相互反应,写出其离子方程式:______________
(4)Y和T两元素的非金属性强弱为Y________T (填“>”“<”或者“=”)。可以验证该结论的方法是___________________
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素所形成含氧酸的酸性
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素与氢气化合的难易程度
E.比较这两种元素气态氢化物的还原性
(5)某化学兴趣小组欲通过实验探究元素N、C、Si 非金属性强弱。实验装置如下:
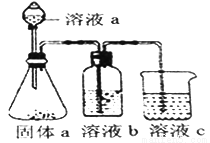
①溶液a和溶液b分别为__________溶液、________溶液(填溶质化学式)
②经验证,N、C、Si的非金属性由强到弱为:__________
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源:2016-2017学年山东省高一下学期开学考试化学试卷(解析版) 题型:填空题
某酸性废液中含有Fe2+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对废液进行处理(所加试剂均稍过量),以回收金属,保护环境。
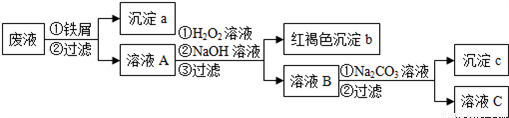
请回答:
(1)沉淀a中含有的单质是_________;
(2)沉淀b的化学式是__________;
(3)沉淀c的化学式是__________;
(4)溶液A与H2O2溶液在酸性条件下反应的离子方程式是_______________。
查看答案和解析>>
科目:高中化学 来源:2017届江西省九江市十校高三第二次联考理科综合化学试卷(解析版) 题型:选择题
25℃时,向100 mL 0.1 mol•L-1 NH4HSO4溶液中滴加0.1 mol•L-1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图(H2SO4视为二元强酸)。下列说法错 误的是( )
误的是( )
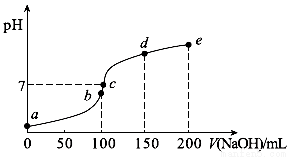
A. a点时溶液的pH<1
B. a点到b点的过程中,溶液的导电能力减弱
C. ab段上的点(不包括a点)均满足关系式:c (NH4+)+c(Na+)<2c(SO42-)
(NH4+)+c(Na+)<2c(SO42-)
D. b点时离子浓度大小顺序为:c(Na+)>c(SO42-)>c(NH4+)> c(H+)> c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一3月月考化学试卷(解析版) 题型:实验题
氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx反应进行了探究。回答下列问题:
(1)氨气的制备
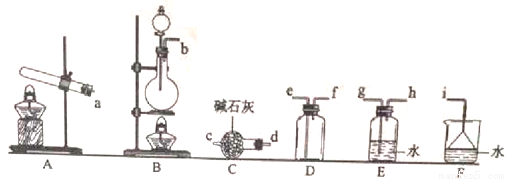
①氨气的发生装置可以选择上图中的_________,反应的化学方程式为_______________。
②预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→______(按气流方向,用小写字母表示)。
(2)氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

操作步骤 | 实验现象 | 解释原因 |
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中 | ①Y管中_____________ | ②反应的化学方程式 ____________ |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
打开K2 | ③_______________ | ④______________ |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一3月月考化学试卷(解析版) 题型:选择题
下列有关说法正确的是( )
A. 次氯酸钙溶液中通入少量SO2气体的离子方程式: Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO
B. CaCl2既含有离子键,又含有非极性键。
C. SO2使KMnO4酸性溶液和滴有酚酞的NaOH溶液褪色的原理相同。
D. 将铁屑溶于过量盐酸后,再加入硝酸锌,会有三价铁生成。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高一3月月考化学试卷(解析版) 题型:选择题
有X、Y两种元素,原子序数≤20,X的原子序数小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是( )
A. 若X的最高价含氧酸为强酸,则X的氢化物溶于水一定显酸性
B. 若Y的最高正价为+m,则X的最高正价一定为+m
C. 若X元素形成的单质是X2,则Y形成的单质一定是Y2
D. 若X(OH)n为强碱,则Y(OH)n也一定为强碱
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高一3月月考化学试卷(解析版) 题型:选择题
下列叙述正确的是( )
A. 碱金属元素是指IA族的所有元素
B. 副族元素没有非金属元素
C. 同周期第ⅡA族和第IIIA族的元素,原子序数之差只能是1或25
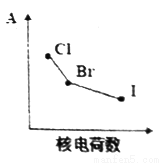
D. 部分卤族元素的某种性质A随核电荷数的变化趋势如右上图所示, 则A可能表示单质的熔沸点
查看答案和解析>>
科目:高中化学 来源:河北省2017届高三下学期三调考试理科综合化学试卷 题型:填空题
聚合氯化铝是一种新型净水剂,其中铝的总浓度(用c表示)包括三类:主要为A l3+的单体形态铝(用Ala表示)总浓度,主要为主要为[AlO4 Al12(OH)24(H2O)12 ]7+的中等聚合形态铝总浓度(用Alb 表示)和Al(OH)3胶体形态铝(用A1c表示)总浓度。
(1)真空碳热还原一氧化法可实现由铝土矿制备金属铝,相关反应的热化学方程式如下:
①Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g)△H1=akJ·mol-1
②3AlCl(g)= 2Al(s)+AlCl3(g) △H2=bkJ·mol-1
则反应Al2O3(s)+33C(s)= 2Al(s)+ 3CO(g)△H=______kJ·mol-1(用含a、b的代数式表尔)。 反应①在常压、1900 ℃ 的高温下才能进行,说明△H______( 填“>”“=”或“<”)。
(1)用膜蒸馏(简称MD)浓缩技术将聚合氯化铝溶液进行浓缩,实验过程中不同浓度聚合氯化铝溶液中铝形态分布(百分数)如下表:
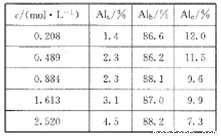
①在一定温度下,c越大,Al(OH)3胶体的百分含量______(填“越大”“越小”或“不变”)。
②若将c=2.520mol/L的聚合氯化铝溶液加水稀释,则稀释过程中发生的主要反应的离子方程式为_____________。
(3)一定条件下,向1.0mol/L的AlCl3溶液中加入0.6 mol/L的NaOH溶液,可制得Alb含量约为86 % 的聚合氯化铝溶液。写出生成[AlO4 Al12(OH)24(H2O)12 ]7+的离子方程式:_______。
(4)已知Al3++4X=2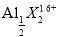 ,X表示显色剂,
,X表示显色剂, 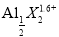 表示有色物质,通过比色分析得到25 ℃时Al3+浓度随时间的变化关系如图所示(初始时X的浓度为0.194mol·L-1)。
表示有色物质,通过比色分析得到25 ℃时Al3+浓度随时间的变化关系如图所示(初始时X的浓度为0.194mol·L-1)。
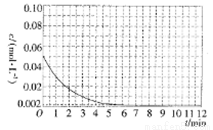
①1min时, 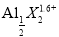 的浓度为___________。
的浓度为___________。
②0~3min内该反应的速率vx=________。
③第9min时,反应达到平衡,K=__________(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2017届新疆乌鲁木齐地区高三第二次诊断性测验化学试卷(解析版) 题型:选择题
己知:①Mn(s)+O2(g)=MnO2(s)△Hl
②S(s)+O2(g)=SO2(g)△H2
③Mn(s)+S(s)+2O2(g)=MnSO4(s)△H3
则下列表述正确的是
A.△H2>0
B.△H3>△H1
C.Mn+SO2==MnO2+S△H=△H2-△H1
D.MnO2(s)+ SO2(g)==MnSO4(s)△H=△H3-△H2-△H1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com