
下列叙述正确的是( )
A.标准状况下任何气体的摩尔体积都是22.4 L
B.1 mol气体的体积若是22.4 L,它必定处于标准状况
C.两种气体的物质的量之比等于其原子个数比
D.标准状况下,1 mol H2和O2的混合气体的体积是22.4 L
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
已知下列反应:Co2O3 + 6HCl(浓) == 2CoCl2 + Cl2↑+ 3H2O (I)
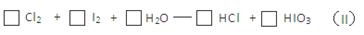
(1)反应(I)中的氧化剂是
(2)根据反应(I)计算,若生成标准状况下33.6L氯气时,电子转移数目是
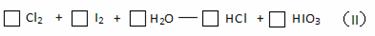 (3)将反应(II)配平
(3)将反应(II)配平
(4)反应(II) 中 发生氧化反应(5)HCl 、I2 、CoCl2三种物质的还原性由强到弱的顺序是
查看答案和解析>>
科目:高中化学 来源: 题型:
利用图示装置收集气体或洗涤气体。
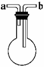
(1)若烧瓶是干燥的,且由a导管进气,可收集比空气________________的气体,如
______________等。
(2)若烧瓶中充满水,则可收集不溶于水的气体,如__________等,气体应从________口进入。
(3)若在烧瓶中放入浓硫酸即可用于干燥气体,则气体应从________口进入。
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列离子方程式相对应的一个化学方程式。
(1) Fe(OH)3+3H+==Fe3++3H2O___________________________
(2)Fe3++3OH—==Fe(OH)3↓___________________________
(3)Ba2++ CO32—==BaCO3↓___________________________
(4) CO32- + 2H+ = CO2↑+ H2O _____________________
(5) NH4+ + OH- = NH3↑+ H2O _____________________________
(6)Mg 2+ + 2OH- = Mg(OH)2↓____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
下列萃取与分液结合进行的操作(用CCl4为萃取剂从碘水中萃取碘)中错误的是( )
A.饱和碘水和CCl4加入分液漏斗中后,盖好玻璃塞,用右手压住分液漏斗上口部,左手握住活塞部分,把分液漏斗倒转过来振荡。
B.静置,分液漏斗中溶液分层,下层呈紫红色上层几乎无色。
C.打开分液漏斗的活塞使全部下层液体沿承接液体的烧杯内壁慢慢流出。
D、最后继续打开活塞另用容器承接并保存上层液体。
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下有:①5.4mL H2O ②5.6L CH4 ③3.01×l023个H2S分子 ④19.6gH2SO4,这些物质中,含分子个数由多到少的顺序是( )
A.③①②④ B.③①④② C.①②③④ D.④②③①
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各物质中含氮原子数最多的是( )
A. 0.1molNH4Cl B. 0.1molNH4NO3 C. 1.204×1023 CO(NH2)2 D. 0.2mol NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
关于SO2的叙述,正确的是( )
A、它可使石蕊试液褪色
B.、等物质的量的Cl2和SO2通入品红溶液中,品红溶液不褪色
C、它能与BaCl2溶液反应生成BaSO3沉淀
D、它与水作用生成H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
环境监测测定水中溶解氧的方法是:①量取25mL水样,迅速加入固定剂MnSO4溶液和碱性KI溶液(含KOH),立即塞好瓶塞,反复振荡,使之充分反应,其反应式为: 2Mn2++O2+4OH-=2MnO(OH)2(该反应极快)②测定:开塞后迅速加入1mL~2mL浓硫酸(提供H+),使之生成I2,再用0.1000mol/L的Na2S2O3溶液滴定(以淀粉为指示剂),消耗V mL。有关反应式为:MnO(OH)2+2I-+4H+=Mn2++I2+3H2O ; I2+2S2O32-=2I-+S4O62-
| 滴定次数 | 待测液的体积/mL | 0.1000mol·L-1 Na2S2O3的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
试回答:(1)消耗Na2S2O3的体积平均值为 ,水中溶解氧的量是(以g/L为单位,保留3位有效数字) 。
(2)滴定(I2和S2O32-反应)以淀粉为指示剂,终点时溶液 。
(3)判断下列操作引起的误差(填“偏大”、“偏小” “无影响”或“无法判断”)
①装标准液的滴定管读数:滴定前平视,滴定后俯视 ,
②未用标准液润洗滴定管____________,
③用固体配制Na2S2O3溶液时,其固体中含有对反应体系无影响的杂质____________,
④待测液的滴定管之前有气泡,取液后无气泡____________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com