

| ||
| △ |
| ||
| △ |
| ||
| ||


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 100 | 150 | 200 |
| 溶解度(g/100gH2O) | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.11 | 0.092 | 0.074 | 0.034 | 0.012 |
| A、氢氧化钙的溶解是放热过程 |
| B、100℃时氢氧化钙的Kxp约等于4×10-6 |
| C、温度升高时氢氧化钙溶解速率加快 |
| D、100℃时pH=12的溶液中c(Ca2+)≤0.04mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
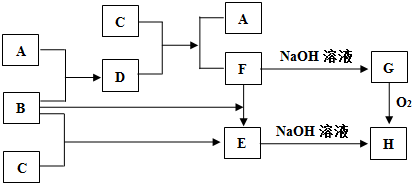
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾和FeCl3可作净水剂 |
| B、为保存FeCl3溶液,要在溶液中加少量盐酸 |
| C、用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 |
| D、氢氟酸用塑料试剂瓶保存而不用玻璃试剂瓶保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)>c(Cl-)>c(OH-)>c(H+) |
| B、c(Na+)=c(Cl-)>c(OH-)>c(H+) |
| C、c(Na+)=c(Cl-)>c(H+)>c(OH-) |
| D、c(Cl-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、υ(H2O)=0.45 mol?L-1?s-1 |
| B、υ(O2)=0.010 mol?L-1?s-1 |
| C、υ(NO)=0.010 mol?L-1?s-1 |
| D、υ(NH3)=0.10 mol?L-1?s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2、D2和T2互称为同位素,它们的化学性质几乎-样 |
| B、二氧化碳、盐酸、氨水分别属于非电解质、强电解质、弱电解质 |
| C、胶体和其它分散系的本质区别是丁达尔效应 |
| D、硅是一种良好的半导体材料,可以制成计算机芯片和硅太阳能电池 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com