
| �ŵ� |
| ��� |
| �ŵ� |
| ��� |
| 1.3g |
| 65g/mol |
| 0.04mol |
| 0.2L |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���û����Һ����һ��������Fe3+��AlO2-��Al3+��CO32- |
| B������Һ�еμӷ�̪��Һ��ʺ�ɫ������BaCl2��Һ����ɫ��ȥ����������ɫ���� |
| C���û����Һ�п϶�����Fe2+��NH4-��SO42-��NO3- |
| D��ͨ��������ɫ��Ӧ����ȷ���Ƿ���I- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
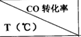 | 1Сʱ | 2Сʱ | 3Сʱ | 4Сʱ |
| T1 | 40% | 70% | 80% | 80% |
| T 2 | 55% | 65% | a1 | a2 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Ʒ�϶�п��������Ӧʽ��Zn-2e-=Zn2+ |
| B�����������缫��ⱥ��ʳ��ˮʱ�������ĵ缫��ӦʽΪ��2Cl--2e-=Cl2�� |
| C����ͭ����ʱ�����Դ�����������Ǵ�ͭ���缫��ӦʽΪCu-2e-=Cu2+ |
| D�����������绯ѧ��ʴ��������Ӧʽ��Fe-2e-=Fe2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���μӷ�̪��NaCl��Һ����ͭ���ϵ�������������ͼ��ʾ��һ��ʱ����������������ش��γ�����ɫ���⣬�����й�˵����ȷ���ǣ�������
���μӷ�̪��NaCl��Һ����ͭ���ϵ�������������ͼ��ʾ��һ��ʱ����������������ش��γ�����ɫ���⣬�����й�˵����ȷ���ǣ�������| A��Һ���µ�ͭ���Ǹ��� |
| B��һ��ʱ���ῴ��Һ���г��ֺ�ɫ |
| C��Һ���е�Na+��ͭ����������Ǩ�� |
| D��Һ���µ�Fe������ԭ��Ӧ������ʴ���˹����л��漰����Ӧ��4Fe��OH��2+2H20+O2=4Fe��OH��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ����� | �ܵ��� | �ǵ���� | ����� |
| ���ڸ�������� | | | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��һ���¶ȡ�ѹǿ�£����ʵ����������ӵĴ�С���� |
| B���¶ȡ�ѹǿһ��ʱ�������������������Ķ��پ��� |
| C������Ħ�������ָ1 mol�κ�������ռ�����Ϊ22.4 L |
| D����ͬ�����壬��������ȣ������������ķ�����һ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������������ķ�Ӧ |
| B�������������þ�ķ�Ӧ |
| C����������������ķ�Ӧ |
| D������Ͱ�ˮ�ķ�Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com