
 ������ȫ����һ���ɴ����������ҡ����巢��������ɣ�
������ȫ����һ���ɴ����������ҡ����巢��������ɣ����� ��1���ٷǽ�����Խǿ��һ������Խ��NԪ��ԭ��2p�ܼ�Ϊ�����ȶ�״̬����һ�����ܸ���ͬ��������Ԫ�صģ�
��NO2-����Nԭ�ӹµ��Ӷ���=$\frac{5+1-2��2}{2}$=1���۲���Ӷ���=2+1=3��
��N2H4��Nԭ���γ�3���Ҽ�������1�Թ¶Ե��ӣ��ӻ������ĿΪ4��N2H4��ˮ���Ӷ��Ǽ��Է��ӣ���������ԭ����N2H4��ˮ����֮���γ������
��2����NiԪ��ԭ�Ӻ��������Ϊ28�������������ԭ����д��������Ų�ʽ��
��Al̼ԭ��ԭ��֮���γɵ�����Cԭ������ԭ��֮���γɵ�������Ϊ�Ҽ���
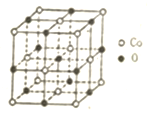
�۸��ݾ�̯�����㾧����Co��Oԭ����Ŀ������ȷ����ѧʽ��
��� �⣺��1���ٷǽ�����Խǿ��һ������Խ��NԪ��ԭ��2p�ܼ�Ϊ�����ȶ�״̬����һ�����ܸ���ͬ��������Ԫ�صģ��ʵ�һ�����ܣ�N��O��H��Na��
�ʴ�Ϊ��N��
��NO2-��Nԭ�ӹµ��Ӷ���=$\frac{5+1-2��2}{2}$=1���۲���Ӷ���=2+1=3��NO2-�ռ乹����V�Σ�
�ʴ�Ϊ��V��
��N2H4��Nԭ���γ�3���Ҽ�������1�Թ¶Ե��ӣ��ӻ������ĿΪ4��Nԭ�Ӳ�ȡsp3�ӻ���N2H4��ˮ���Ӷ��Ǽ��Է��ӣ���������ԭ����N2H4��ˮ����֮���γ������N2H4��������ˮ��
�ʴ�Ϊ��sp3��N2H4��ˮ���Ӷ��Ǽ��Է��ӣ���������ԭ����N2H4��ˮ����֮���γ������
��2����NiԪ��ԭ�Ӻ��������Ϊ28�������������ԭ������������Ų�ʽΪ1s22s22p63s23p63d84s2��
�ʴ�Ϊ��1s22s22p63s23p63d84s2��
��Al̼ԭ��ԭ��֮���γɵ�����Cԭ������ԭ��֮���γɵ�������Ϊ�Ҽ��������к��еĦҼ�����ĿΪ12��
�ʴ�Ϊ��12��
�۾�����Coԭ����ĿΪ6��$\frac{1}{2}$+8��$\frac{1}{8}$=4��Oԭ����Ŀ=1+12��$\frac{1}{4}$=4���ʸû�����Ļ�ѧʽΪCoO��
�ʴ�Ϊ��CoO��
���� �����Ƕ����ʽṹ�����ʵĿ��飬�漰�����ܡ��ӻ���ʽ��ռ乹���жϡ����ӽṹ�����ʡ���ѧ������������Ų�����������ȣ�ע��ͬ����Ԫ�ص�һ�������쳣������Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Ũ����մ��Ƥ����ʱ���������ô�����ˮ��ϴ��Ȼ����Ϳ��3%��5%��NaHCO3��Һ | |
| B�� | ȡ�û�ѧҩƷʱ��Ӧ�ر�ע��۲�ҩƷ��װ�����ϵİ�ȫ��ʾ��־ | |
| C�� | ���Ǹ������������ȣ���Ҫ�ӵ�ʯ�������Է�����ը�� | |
| D�� | ���κλ�ѧҩƷ����ζ�����ܽ����Ӵս�ҩƷ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeS04•7H20-�̷� | B�� | Na2O2-��� | C�� | BaC03-�ؾ�ʯ | D�� | C6Hl206-���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
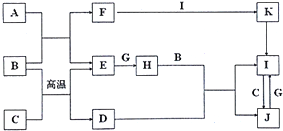
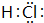
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
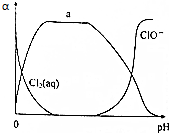 �ȼ��仯����������ˮ�������߱��ʵȷ���Ӧ�ù㷺��
�ȼ��仯����������ˮ�������߱��ʵȷ���Ӧ�ù㷺���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������������ϡ���ᷴӦ��2Fe+6H+��2Fe3++3H2�� | |
| B�� | �Ȼ�������Һ��ͨ������������Fe2++Cl2��Fe3++2Cl- | |
| C�� | ������������������Һ��Ӧ��Al2O3+2OH-=2AlO2-+H2O | |
| D�� | �Ȼ�����Һ�м�������İ�ˮ��Al3++3OH-��Al��OH��3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ϊ����ĸ���� | B�� | �����²�������������Ӧ | ||
| C�� | ���������ϣ����ǻ��� | D�� | ��ҵ����Ҫ���ýӴ����Ʊ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��C��ʯī��s���TC�����ʯ��s����H��0������ʯ��ʯī�ȶ� | |
| B�� | ������������������ǹ���ֱ���ȫȼ�գ����߷ų��������� | |
| C�� | ��ͬ���Ũ�Ⱦ�Ϊ0.1 mol/L ����ʹ�����Һ�ֱ���������NaOHϡ��Һ��Ӧ��ǰ�߷ų������� | |
| D�� | ������ȼ����Ϊ285.8 kJ/mol��������ȼ�յ��Ȼ�ѧ����ʽΪ��2H2��g��+O2��g���T2H2O��l����H=-285.8 kJ/mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com