
| A、氧化性:Cl2>Fe3+>I2>SO42- |
| B、还原性:SO2>I->Fe2++>Cl- |
| C、反应:Cl2+2I-=2Cl-+I2 可发生 |
| D、反应:Cl2+SO2+2H2O=4H++SO42-+2Cl-不可发生 |


科目:高中化学 来源: 题型:
| A、H+、Ba2+、SO42-、ClO- |
| B、Ca2+、Mg2+、NO3-、OH- |
| C、K+、Mg2+、Cl-、SO42- |
| D、Ag+、Na+、NO3-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶于500mL水中 |
| B、溶于1L水中 |
| C、溶解后溶液的总体积为500ml |
| D、溶解后溶液的总体积为1L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所用NaOH已经潮解 |
| B、定容时俯视 |
| C、未洗涤烧杯及玻璃棒 |
| D、称量时误用“左码右物” |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
| B、pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| C、pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
| D、0.1mol?L-1CH3COONa溶液中:c(OH-)=c(CH3COOH)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
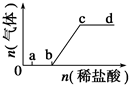 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )| A、a点对应的溶液中:Na+、OH-、SO42-、NO3- |
| B、b点对应的溶液中:Al3+、Fe3+、SCN-、Cl- |
| C、c点对应的溶液中:Na+、Ca2+、NO3-、Cl- |
| D、d点对应的溶液中:Fe2+、Na+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2C=CH-CH=CH2 1,3-二丁烯 |
B、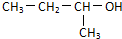 1-甲基-1-丙醇 1-甲基-1-丙醇 |
C、 2,6-二甲基-5-乙基庚烷 2,6-二甲基-5-乙基庚烷 |
D、 2-乙基-1-丁烯 2-乙基-1-丁烯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com