
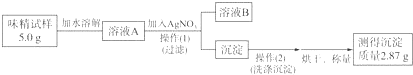
分析 ①依据溶液中分离出固体的实验操作是过滤,依据过滤实验装置分析需要的玻璃仪器;
②依据元素守恒计算氯化钠的含量和标准NaCl含量≤20%”比较分析判断;
③依据沉淀质量计算物质的量根据氯元素守恒得到氯化钠物质的量,依据c=$\frac{n}{V}$计算得到溶液浓.
解答 解:①溶液中分离出固体的实验操作是过滤,需要的玻璃仪器为普通漏斗 烧杯 玻璃棒;
故答案为:普通漏斗 烧杯 玻璃棒;
②流程分析,生成的氯化银沉淀质量2.87g,物质的量=$\frac{2.87g}{143.5g/mol}$=0.02mol,则样品中氯化钠物质的量为2mol,质量分数=$\frac{0.02mol×58.5g/mol}{5.0g}$×100%=23.4%>20%,所以味精中NaCl的质量分数不符合其包装上标注的标准;
故答案为:23.4%;不符合;
③依据上述计算可知A溶液中含有氯化钠物质的量为0.02mol,溶液A为50mL,则溶液A中NaCl的物质的量浓度=$\frac{0.02mol}{0.05L}$=0.4mol/L;
答:如果溶液A为50mL,则溶液A中NaCl的物质的量浓度是0.4mol/L.
点评 本题考查了物质组成的实验测定实验设计和计算应用,主要是实验基本操作的应用,掌握基础是解题关键,题目难度中等


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.1mol | B. | 0.4mol | C. | 1.1mol | D. | 1.6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
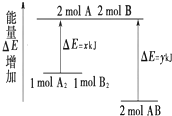
| A. | 该反应是吸热反应 | |
| B. | 断裂1molA-A键和1mol B-B 键放出xkJ能量 | |
| C. | 断裂2molA-B键需要吸收(y-x)kJ的能量 | |
| D. | 1molA2和1molB2的总能量高于2molAB的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放热183 kJ | B. | 放热91.5 kJ | C. | 吸热183 kJ | D. | 吸热91.5 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ①可能形成AgBr沉淀 | B. | ①一定能有效分离Cl-与Br- | ||
| C. | ②一定不能形成AgCl沉淀 | D. | ②一定能有效分离Cl-与Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
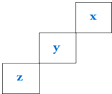
| A. | 元素Z一定是长周期元素,且既有金属性又有非金属性 | |
| B. | 三种元素中X元素的最高价氧化物对应的水化物酸性最强 | |
| C. | 三种元素中X元素的气态氢化物还原性最弱 | |
| D. | Y元素可形成多种不同的单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的$\frac{1}{4}$.
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的$\frac{1}{4}$.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com