
【题目】某学生做了如下4个实验:
①在铝盐溶液中逐滴加入稀氨水直至过量;
②在明矾溶液中加入氢氧化钡溶液直至过量;
③在含少量氢氧化钠的偏铝酸钠溶液中通入二氧化碳直至过量;
④在少量盐酸的氯化铝溶液中加入氢氧化钠至过量。
在4个图像,纵坐标为沉淀物质的量,横坐标为溶液中加入物质的物质的量,上述实验与图像对应关系正确的是( )
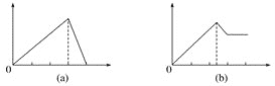
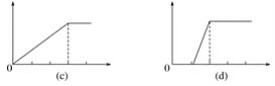
A.①-(d)B.②-(b)C.③-(c)D.④-(a)
【答案】B
【解析】
①铝盐中滴入稀氨水生成沉淀氢氧化铝,根据氢氧化铝不溶于弱碱氨水,铝盐反应完后沉淀量不再变化;反应为Al3++3NH3H2O=Al(OH)3↓+3NH4+,根据定量关系,故d不符合,故A错误;
②明矾溶液中的铝离子与滴入氢氧化钡溶液,反应生成硫酸钡和氢氧化铝沉淀,铝离子反应完后,继续滴入氢氧化钠溶液,氢氧化铝沉淀溶解而硫酸钡不溶;最后剩余硫酸钡,故b符合,故B正确;
③在含少量NaOH的偏铝酸钠溶液中通入CO2直至过量,CO2先与氢氧化钠反应,不产生沉淀,反应完后再与偏铝酸钠溶液反应生成沉淀至达到最大值后不再变化,发生的反应为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故c不符合,故C错误;
④在少量盐酸的氯化铝溶液中加入NaOH至过量,氢氧化钠先与盐酸反应,无沉淀生成,后与氯化铝溶液反应完后,生成沉淀达最大值后又逐渐溶解,故a不符合,故D错误;
故答案为B。


科目:高中化学 来源: 题型:
【题目】将11.2g铁粉投入200mL的稀硫酸中,充分反应后,铁粉完全溶解。(假设反应后溶液体积不发生变化,写出计算过程)
⑴求标准状况下产生气体的体积。(已知:Fe+H2SO4=FeSO4+H2↑)_____________
⑵求反应后溶液中FeSO4的物质的量浓度。_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,22.4LHF的分子数约为NA
B.将1molCl2通入水中,HClO、Cl-、ClO-的粒子数之和为2NA
C.氢氧燃料电池正极消耗22.4L(标准状况)气体时,线路中通过电子数目为2NA
D.若用惰性电极电解足量CuSO4溶液后,加入0.1molCuO可以复原,则电解时转移电子数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家已研制出一种可替代锂电池的“可充室温Na-CO2电池”,该电池结构如图所示。电极材料为钠金属片和碳纳米管,电解液为高氯酸钠-四甘醇二甲醚。下列说法错误的是( )
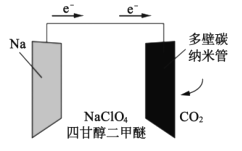
A.电池放电时钠金属片发生氧化反应
B.电池工作时,外电路流过0.01mol电子,负极材料减重0.23g
C.碳纳米管的作用主要是导电及吸附CO2,电池充电时,应该与直流电源的正极相连
D.放电时负极反应为:C+2Na2CO3-4e-=3CO2↑+4Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学实验中常见的制备气体并进行某些物质的检验和性质实验的装置,A是制备气体的装置,C、D、E、F中盛装的液体可能相同,也可能不同。试回答:
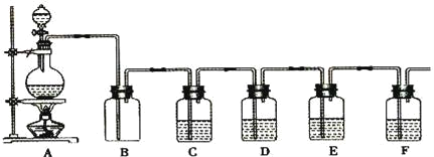
(1)如果A中的固体物质是碳,分液漏斗中盛装的是浓硫酸,试写出发生的化学反应方程式:____,若要检验生成的产物,则B、C、D、E、F中应分别加入的试剂为__、__、__、__、__,E中试剂和C中相同,E中试剂所起的作用__,B装置除可检出某产物外,还可起到__作用。
(2)若进行上述实验时在F中得到10.0 g固体,则A中发生反应转移的电子数为__个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据下图关系推断:

(1)写出化学式:X_______,A________,B_______。
(2)实验室收集气体D和F的方法依次是_______法、________法。
(3)写出C→E的化学方程式:____________。
(4)请写出A与E反应生成D的化学方程式:_______________
(5)检验物质A的方法和现象是________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用如图所示装置可以在铜牌表面电镀一层银。下列有关说法正确的是( )

A.银片电极上发生还原反应,电极反应为Ag++e-=Ag
B.反应过程中电能全部转化为化学能
C.撤去电源并构成回路后,发生铜的吸氧腐蚀
D.当电镀一段时间后,将电源反接,铜牌不可能恢复如初
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为原子序数依次增大的四种短周期元素,已知C、D元素的原子序数之和是A、B元素的原子序数之和的3倍,且C、D元素是同主族元素。甲、乙、丙、丁、戊五种二元化合物的组成如下表:

物质间存在反应:甲+乙→单质B+丙;丁+戊→单质D(淡黄色固体)+丙。下列说法正确的是( )
A.甲、乙、丙、丁、戊均为只含极性键的极性分子
B.原子半径:D>B>C;电负性:B>C>D
C.可用酒精洗涤粘在容器内壁上的单质D
D.若2mol甲与3mol乙恰好反应生成2.5mol单质B,则乙为双原子分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com