
| A、若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由“C(石墨)=C(金刚石)△H=1.9kJ/mol”可知,金刚石比石墨稳定 |
| C、已知2C(s)+2O2 (g)═2 CO2(g)△H1;2C(s)+O2 (g)═2 CO (g)△H2则△H1>△H2 |
| D、在稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,若将含1molCH3COOH与含1mol NaOH的溶液混合,放出的热量小于57.3kJ |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、漂白粉长期暴露在空气中会变质失效 |
| B、雾霾天车灯照射的光亮通路属于丁达尔现象 |
| C、硬铝属于合金材料,瓷器属于硅酸盐制品 |
| D、不锈钢具有较强的抗腐蚀性,是因为在钢铁表面镀上了金属铬 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2(g)+O2(g)=2H2O(g),△H1; 2H2(g)+O2(g)=2H2O(l),△H2 |
| B、H2(g)+Cl2(g)=2HCl(g),△H1; 2H2(g)+2Cl2(g)=4HCl(g),△H2 |
| C、C(s)+1/2O2(g)=CO(g),△H1; C(s)+O2(g)=CO2(g),△H2 |
| D、S(g)+O2(g)=SO2(g),△H1; S(s)+O2(g)=SO2(g),△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
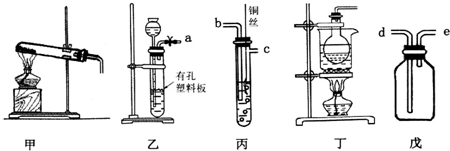
 用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图所示从下表中选出正确选项( )
用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图所示从下表中选出正确选项( )| 选项 | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 |
| A | 碱 | 酸 | 石蕊 | 乙 |
| B | 酸 | 碱 | 酚酞 | 甲 |
| C | 碱 | 酸 | 甲基橙 | 乙 |
| D | 酸 | 碱 | 酚酞 | 乙 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、卤化氢中,以HF沸点最高,是由于HF分子间存在氢键 |
| B、H2O的沸点比HF的高,是由于水中形成的氢键多 |
| C、氨水中有分子间氢键 |
| D、氢键X-H…Y的三个原子总在一条直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、28g乙烯和28g丙烯分子中均含有6NA个共用电子对 |
| B、在熔融状态下,1molNaHSO4完全电离出的阳离子数目为2NA |
| C、7.8gNa2O2中含有阴离子数目为0.2NA |
| D、在含4molC=O键的干冰晶体中,碳原子的数目为4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com