
【题目】X、Y、Z、W为短周期元素,它们在周期表中相对位置如图所示。若Z的原子序数是Y的原子序数的2倍,下列说法正确的是

A. 简单离子半径:X>Y>ZB. 氢化物的稳定性:Z<Y
C. 原子半径:W>Z>YD. 最高价氧化物对应水化物的酸性:W<Z
【答案】B
【解析】
X、Y、Z、W均为短周期元素,Z与Y同主族,短周期中两者原子序数相差8,Z的原子序数是Y的原子序数的2倍,则Y为氧元素,根据X、Y、Z、W在周期表中相对位置可知,X为氮元素,Z为硫元素,W为氯元素,据此分析。
X、Y、Z、W均为短周期元素,Z与Y同主族,短周期中两者原子序数相差8,Z的原子序数是Y的原子序数的2倍,则Y为氧元素,根据X、Y、Z、W在周期表中相对位置可知,X为氮元素,Z为硫元素,W为氯元素。
A. Z离子比X、Y离子多一个电子层,半径最大,X、Y离子具有相同电子层结构,核电荷数越大半径越小,故简单离子半径: Z >X>Y,选项A错误;
B. 非金属性越强,气态氢化物的稳定性越强,因非金属性Z<Y,故氢化物的稳定性:Z<Y,选项B正确;
C. 同周期随原子序数增大原子半径减小,电子层越多原子半径越大,故原子半径Z>W>Y,选项C错误;
D.Z、W同周期,随原子序数增大元素非金属性增强,最高价含氧酸的酸性增强,选项D错误。
答案选B。


科目:高中化学 来源: 题型:
【题目】有下列物质:①氮氧化物、②未完全燃烧的碳氢化合物、③含铅化合物、④二氧化硫、⑤一氧化碳,其中属于汽车尾气成分的是( )
A.①②③④
B.①②③⑤
C.②③④⑤
D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

(1)氢氧燃料电池的在导线中电流的方向为由______(用a、b表示)。
(2)负极反应式为______,正极反应式为___________。
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ 2Li+H2![]() 2LiH Ⅱ LiH+H2O=LiOH+H2↑
2LiH Ⅱ LiH+H2O=LiOH+H2↑
①反应Ⅰ中的还原剂是_________,反应Ⅱ中的氧化剂是_____。
②已知LiH固体密度为0.82g·cm-3,用锂吸收224 L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为______。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为___mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作规范且能达到目的的是
目的 | 操作 | |
A. | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩余盐酸放入锥形瓶 |
B. | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
C. | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
D. | 配制浓度为0.010 | 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是( )


A. ①是其他条件一定时,反应速率随温度变化的图像,正反应ΔH<0
B. ②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图像
C. ③是在有无催化剂存在下建立的平衡过程图像,a是使用催化剂时的曲线
D. ④是一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强p1>p2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
A. NaCl和HCl B. CO2和SiO2 C. SO2和H2O D. CCl4和NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0.100 mol·L-1的NaOH溶液滴定10.00 mL浓度均为0.100 mol·L-1 的盐酸和 CH3COOH溶液。利用传感器测得滴定过程中溶液 的电导率如图所示。下列说法不正确的是
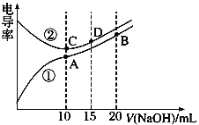
A. A点溶液中:c(CH3COO-)+c(OH-)-c(H+)= 0.0500 mol·L-1
B. 曲线②代表滴定CH3COOH溶液的曲线
C. 在相同温度下,A、B、C三点溶液中水的电离程度: A>C>B
D. B点溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小明同学设计了如图所示装置来探究铜跟浓硫酸的反应。
先关闭活塞a,加热至烧瓶中不再有气泡产生时,反应停止,此时烧瓶中铜片仍有剩余。再打开活塞a,将气球中的氧气缓缓挤入烧瓶,铜片慢慢消失。

(1)请写出上述过程A装置中所涉及的化学反应方程式。
________________________
_________________________
(2)实验中加热至烧瓶中不再有气泡产生时,反应停止,此时烧瓶中铜片为什么有剩余?请简述其原因是:___________。
(3)老师认为实验中B装置设计有误,请你帮助小明进行修改:___________。
(4)B中所收集到的气体既具有氧化性又具有还原性,请写出该气体与O2反应的化学方程式:______。
(5)装置C中应盛放____溶液,其作用是:____,所发生的离子方程式为:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂选用的试剂或操作方法正确的是
物质 | 杂质 | 除去杂质选用的试剂或操作方法 | |
A | KNO3溶液 | KOH | 加入适量氯化铁溶液,并过滤 |
B | FeSO4溶液 | CuSO4 | 加入过量铜粉,并过滤 |
C | H2 | CO2 | 先后通过盛有氢氧化钠溶液和浓硫酸的洗气瓶 |
D | 铁粉 | 铜粉 | 加入足量稀硫酸过滤 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com