
分析 (1)在水溶液里或熔融状态下能导电的化合物是电解质,包括酸、碱、盐、活泼金属氧化物和水;
在水溶液里和熔融状态下都不能导电的化合物是非电解质,包括一些非金属氧化物、氨气、大多数有机物(如蔗糖、酒精等);
物质导电的条件:含有自由移动的离子或自由电子;
(2)除去NaCl中的Na2SO4,先加氯化钡除去硫酸根离子,再利用碳酸钠除去过量的钡离子,最后加盐酸除去过量的碳酸钠,以此来解答.
解答 解:(1)①液态SO3 不含自由移动的离子或自由电子,不导电;本身不能电离,属于非电解质;
②BaCO3固体不含自由移动的离子或自由电子,不导电;熔融状态下能够导电,属于电解质;
③酒精不含自由移动的离子或自由电子,不导电;在水溶液里和熔融状态下都不能导电的化合物,是非电解质;
④盐酸含有自由离子,能够导电;是混合物,既不是电解质,也不是非电解质;
⑤汞含自由电子,能够导电;是单质,既不是电解质,也不是非电解质;
⑥NaCl晶体,不含自由移动的离子或自由电子,不导电;在水溶液里或熔融状态下能导电的化合物是电解质;
⑦纯醋酸不含自由移动的离子或自由电子,不导电;在水溶液能导电的化合物是电解质;
⑧水,含有自由移动的离子,能够导电;在水溶液能导电的化合物是电解质;
能导电的是:④⑤⑧;属于电解质的有②⑥⑦⑧;属于非电解质①③;
故答案为:④⑤⑧;②⑥⑦⑧;①③;
(2)除去NaCl中的Na2SO4,先加足量氯化钡除去硫酸根离子,再利用足量碳酸钠除去过量的钡离子,最后加适量盐酸除去过量的碳酸钠,则依次加入的溶液的溶质为BaCl2、Na2CO3、HCl,故答案为:BaCl2;Na2CO3;HCl.
点评 本题考查了电解质、非电解质判断,电解质以及混合物分离提纯,明确电解质、非电解质概念是解题关键,注意单质、混合物既不是电解质也不是非电解质,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 2NaBr+Cl2═2NaCl+Br2 | |
| B. | AlCl3+3NaAlO2+6H2O═4Al(OH)3↓+3NaCl | |
| C. | 2H2S+SO2═2H2O+3S↓ | |
| D. | C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3、MgC12 | B. | NH4HCO3、AlC13 | C. | (NH4)2CO3、BaCl2 | D. | NH4HCO3、MgC12 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
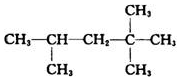 ,它是汽油燃烧品质抗震性能的参照物,用系统命名法对它命名2,2,4-三甲基戊烷,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:
,它是汽油燃烧品质抗震性能的参照物,用系统命名法对它命名2,2,4-三甲基戊烷,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为: ;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为CH2=C(CH3)CH2C(CH3)3或(CH3)2C=CH(CH3)3.
;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为CH2=C(CH3)CH2C(CH3)3或(CH3)2C=CH(CH3)3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50 mL 0.2 mol/L的NaCl溶液 | B. | 100 mL 0.2 mol/L的NaCl溶液 | ||
| C. | 25 mL 0.1 mol/L的Na2SO4溶液 | D. | 50 mL 0.1 mol/L的NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L盐酸含有NA个HCl分子 | |
| B. | 常温常压下,22.4LCO2和SO2混合气体含有2NA个O原子 | |
| C. | 常温常压下,8gCH4含有5NA个电子 | |
| D. | 1mol/LNaCl溶液中含有NA个Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com