
700℃时,向容枳为2L的密闭容器中充入一定量的CO和H2O发生反应:
CO(g)+H2O(g) 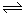 CO2+H2(g)
CO2+H2(g)
反应过程中测定的部分数据见表。下列说法正确的是

A.反应在t1min内的平均速率为v (H2)=0.4/t1 mol·L-1·min-1
B.其他条件不变,起始时向容器中充入0.60molCO和1.20 mo1H2O,到达平衡时,n(CO2)=0.40 mol
C.其他条件不变,向平衡体系中再通入0.2molH2O,达到新平衡时CO转化率减小
D.温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应
B
【解析】
试题分析:A、在t1min内水蒸气的物质的量减少(0.60-0.20)mol=0.40mol,则氢气的物质的量增加0.40mol,所以v (H2)=0.40mol/2L/t1min=0.2/t1 mol·L-1·min-1,错误;B、t1时刻与t2时刻CO的物质的量相同,都是0.8mol,所以t1时达到平衡状态,c(CO)=0.8mol/2L=0.4mol/L,c(H2O)=0.2mol/2L=0.1mol/L,c(CO2)=c(H2)=0.4mol/2L=0.2mol/L,则该反应的平衡常数K= c(CO2)·c(H2)/ c(CO)·c(H2O)=1,其他条件不变,起始时向容器中充入0.60molCO和1.20 mo1H2O,设二氧化碳的浓度为x,则
CO(g)+H2O(g)  CO2+H2(g)
CO2+H2(g)
开始(mol/L) 0.3 0.6
转化(mol/L) x x x x
平衡(mol/L) 0.3-x 0.6-x x x
所以x·x/(0.3-x)·(0.6-x)=1,解得x=0.2mol/L,则,n(CO2)= 0.2mol/L×2L=0.4mol,正确;C、其他条件不变,向平衡体系中再通入0.2molH2O,平衡正向移动,达到新平衡时CO转化率增大,错误;D、温度升至800℃,上述反应平衡常数为0.64,说明升高温度,平衡常数减小,则升高温度,平衡逆向移动,所以正反应是放热反应,错误,答案选B。
考点:考查反应速率、平衡常数的计算与应用,化学平衡移动的判断


 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源:2014-2015学年上海市长宁区高三上学期教学质量检测化学试卷(解析版) 题型:填空题
(本题共10分)3-对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下:

已知:HCHO+CH3CHO CH2=CHCHO+H2O。
CH2=CHCHO+H2O。
45.A的同分异构体有多种,写出其中遇FeCl3溶液显紫色且苯环上有两个取代基的有机物结构简式____ 。B中含氧官能团的名称为_____________。
46.试剂C可选用下列中的_____________。
A、溴水 B、银氨溶液
C、酸性KMnO4溶液 D、新制Cu(OH)2悬浊液
47. 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为_________________________________________________________。
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为_________________________________________________________。
48.E在一定条件下可以生成高聚物F,F的结构简式为______________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省等四校高三第二次联考化学试卷(解析版) 题型:填空题
(9分)已知物质A、B、C、D、E是由短周期元素构成的单质或化合物,它们可发生如图所示的转化关系:

(1)若条件①为点燃,目前60%的B都是从海水中提取的,气体D可以使湿润的红色石蕊试纸变蓝,写出C与H2O反应的化学方程式_____________。将气体D作为燃料电池的燃料源可以制成D—空气燃料电池系统,总反应式为:D+O2 A+H2O(未配平),写出此碱性燃料电池的负极反应式:________________。
A+H2O(未配平),写出此碱性燃料电池的负极反应式:________________。
(2)若条件①为加热,E是一种两性氢氧化物,气体D是一种有臭鸡蛋气味的气体,其水溶液是还原性酸,则C为____________(写化学式)。
(3)若条件①为常温,B和D为同种无色气体,常温下E的浓溶液可以使Fe钝化,写出少量Fe粉与E的稀溶液反应的离子方程式:_________________________________。
已知常温下1molC与H2O反应生成气体D和E溶液放出46kJ热量,写出C与水反应生成D和E的热化学方程式:________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省等四校高三第二次联考化学试卷(解析版) 题型:选择题
下列判断错误的是
A.沸点:NH3>PH3>AsH3
B.结合质子的能力:OH->CH3COO->Cl-
C.酸性:HClO4 >H2SO4 >H3PO4
D.碱性:NaOH >Mg(OH)2 >Al(OH)3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东师大附中高三第四次模拟考试理综化学试卷(解析版) 题型:填空题
(17分)氢气和氨气都属于无碳清洁能。
(1)某些合金可用于储存氢,金属储氢的原理可表示为:M(s)+xH2 MH2x(s) △H<0(M表示某种合金)
MH2x(s) △H<0(M表示某种合金)
下图表示温度分别为T1、T2时,最大吸氢量与氢气压强的关系。则下列说法中,正确的是_____________

a.T1>T2
b.增大氢气压强,加快氢气的吸收速率
c.增大M的量,上述平衡向右移动
d.在恒温、恒容容器中,达平衡后充入H2,再次平衡后的压强增大
(2)以熔融碳酸盐为电解质,稀土金属材料为电极组成氢氧燃料电池(如装置甲所示),其中负极通入H2,正极通入O2和CO2的混合气体。乙装置中a、b为石墨电极,电解过程中,b极质量增加。

①工作过程中,甲装置中d电极上的电极反应式为_____________________________。
②若用该装置电解精炼铜,则b极接____(填“粗铜”或“精铜”);若用该装置给铁制品上镀铜,则____(填“a”或“b”)极可用惰性电极(如Pt电极),若电镀量较大,需要经常补充或更换的是_______。
(3)氨在氧气中燃烧,生成水和一种空气组成成分的单质。
已知:N2(g)十3H2(g)  2NH3(g) △H=
2NH3(g) △H= 92.4kJ·mol-1
92.4kJ·mol-1
2H2(g)十O2(g)=2H2O(1) △H= 572KJ·mo1-1
572KJ·mo1-1
试写出氨气在氧气中燃烧生成液态水的热化学方程式___________________。
(4)在一定条件下,将lmotN2和3molH2混台于一个10L的密闭容器中发生反应:
N2(g)十3H2(g)  2NH3(g)
2NH3(g)
5min后达到平衡,平衡时氮气的转化率为 。
。
①该反应的平衡常数K=________,(用含 的代数式表示)
的代数式表示)
②从反应开始到平衡时N2的消耗速率v(N2)=____mo1·L-1·min-1。(用含 的代数式表示)
的代数式表示)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省曲阜市高三上学期期中考试化学试卷(解析版) 题型:实验题
(12分)金属单质及其化合物在生产生活中应用非常广泛,废旧金属的回收利用是重要研究课题。某学习小组在实验室中模拟利用含铜废料(主要成分为Cu和CuO,还有少量的A1,Fe及其氧化物)生产胆矾,其实验方案如下:

(1)上述流程中,操作1所得“滤液’‘的主要成分为_____________;
(2)酸溶后所得溶液中的榕质主要有_____________;
(3)请写出酸溶过程单质铜发生反应的离子方程式___________;该反应中氧化剂与还原剂的物质的量之比为______________;
(4)试剂可以是________________;
(5)操作3是一系列操作.其操作为______________、冷却结晶、过滤、___________、小心干燥。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省曲阜市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列关干氧化物的各项叙述正确的是
①酸性氧化物不一定是非金属氧化物 ②非金属氧化物肯定是酸性氧化物
③碱性氧化物肯定是金属氧化物 ④金属氧化物肯定是喊性氧化物
⑤酸性氧化物均可与水反应生成相应的酸
⑥与水反应生成酸的氧化物不一定是酸性氧化物,与水反应生成碱的氧化物不一定是碱住氧化物
⑦不能跟酸反应的氧化物一定能跟碱反应
A.①③⑥ B.①②⑤⑦ C.③④⑤ D.①②⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三1月检测化学试卷(解析版) 题型:选择题
向100mL pH=0的硫酸和硝酸混合溶液中投入3.84g铜粉,微热使反应充分完成后,生成NO气体448mL(标准状况)。则反应前的混合溶液中含硝酸的物质的量为
A.0.02mol B.0.08mol C.0.10mol D.0.16mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省常州市高三上学期期末化学试卷(解析版) 题型:填空题
(12分)A、B、C、D、E、F为原子序数依次增大的短周期主族元素。A、F原子的最外层电子数均等于其周期序数,F原子的电子层数是A的3倍;B原子核外电子分处3个不同能级且每个能级上的电子数相同;A与C形成的分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对,E电负性小于F。
(1)写出B的基态原子的核外电子排布式: 。
(2)A、C形成的分子极易溶于水,其主要原因是 。与该分子互为等电子体的阳离子为 。
(3)比较E、F的第一电离能:E F。(选填“>”或“<”)
(4)BD2在高温高压下所形成的晶胞如图所示 。该晶体的类型属于 (选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子的杂化形式为 。
。该晶体的类型属于 (选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子的杂化形式为 。

(5)光谱证实单质F与强碱性溶液反应有[F(OH)4]-生成,则[F(OH)4]-中存在 。(填序号)
a.共价键
b.非极性键
c.配位键
d.σ键
e.π键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com