
����Ŀ�������������γɹ⻯ѧ�������������Ҫԭ�������о�������йص�����������ʣ���ش��������⣺
��1������ NOx��һ�ַ��������ü������ԭNOx��
CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) K1
CH4 (g)+2NO2(g) = N2 (g)+CO2(g)+2H2O(g) K2
CH4 (g)+4NO(g) = 2N2 (g)+CO2(g)+2H2O(g) K3
K1��K2��K3����Ϊ������Ӧ��ƽ�ⳣ������K3=______����K1��K2��ʾ��
��2���ں����ܱ�������ͨ������ʵ�����CO��NO����һ�������·�����Ӧ��2CO(g)+2NO(g)![]() N2(g)+2CO2 (g)�����NO��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
N2(g)+2CO2 (g)�����NO��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
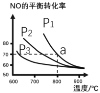
����÷�Ӧ����H ________0��������������������=������
�ڶ������෴Ӧ����ij���(B)��ƽ���ѹǿ p(B)�������ʵ���Ũ�� c(B) Ҳ�ɱ�ʾƽ�ⳣ��kp����÷�Ӧ��ƽ�ⳣ������ʽkp=________�����p1 =1.65MPa����a���ƽ�ⳣ��kp =_________��MPa��1 (������� 3 λ��Ч���֣���ѹ=��ѹ�����ʵ�������)��
��Ϊ̽��������Ũ�ȵĹ�ϵ����ʵ���У��������ʵ�����ݣ����Ի�����2��������Ũ�ȹ�ϵ����: v��~c(NO)��v��~c(CO2 )
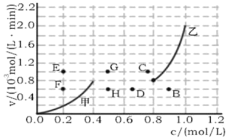
�������� v��~c(NO)���Ӧ����ͼ������________(����������������)�������ͷ�Ӧ��ϵ���¶ȣ���Ӧһ��ʱ������´ﵽƽ�⣬v����v����Ӧ��ƽ���ֱ�Ϊ______(����ĸ)��
��3�����õ绯ѧԭ������NO2��O2�����ڵ�KNO3�Ƴ�ȼ�ϵ�أ�ģ�ҵ��ⷨ��������Cr2O72�ķ�ˮ����ͼ��ʾ������������Һ������Ӧ��Cr2O72+6Fe2++14H+=2Cr3++6Fe3+ +7H2O��
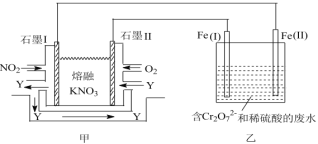
�ټ�ع���ʱ��Y�����壬��ѭ��ʹ�á���ʯīI���������ĵ缫��ӦʽΪ________���ҳ��е�pH________���������������С����������������
�ڹ���ʱ������ͬ�����£��׳������ĵ�O2��NO2�����_____��
��4����֪H3PO4Ϊ��Ԫ�ᣬKa1=7.0��103mol��L1��Ka2=6.2��108 mol��L1��Ka3=4.5��1013mol��L 1���� Na2HPO4ˮ��Һ��________�����������������������������ԣ���Ka��Kh����Դ�С��˵���ж�����________________��
���𰸡�![]() ��
�� ![]() 21.2��MPa��-1 �� D��H NO2+NO3--e-=N2O5 ��� 1��4 �� Na2HPO4��ˮ��ƽ�ⳣ��Kh2=
21.2��MPa��-1 �� D��H NO2+NO3--e-=N2O5 ��� 1��4 �� Na2HPO4��ˮ��ƽ�ⳣ��Kh2=![]() =
=![]() =
=![]() =1.6��10��7��Ka3=4.5��1013��HPO42-��ˮ��̶ȴ��ڵ���̶ȣ��ʶ��Լ���
=1.6��10��7��Ka3=4.5��1013��HPO42-��ˮ��̶ȴ��ڵ���̶ȣ��ʶ��Լ���
��������
��1�����ݸ�˹���ɺ�ƽ�ⳣ����ʽ����ɵã�
��2���������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ���
�����ݷ�Ӧ��ƽ�ⳣ��������д���ɣ�������ʽ�õ����ʵ����ʵ������������빫ʽ����ɵã�
��NO�Ƿ�Ӧ�CO2��������淴Ӧ���У�NOŨ�ȼ�С��CO2Ũ�������ͷ�Ӧ��ϵ���¶ȣ�v��~c(NO)��v��~c(CO2 )����С���÷�ӦΪ���ȷ�Ӧ��ƽ��������Ӧ�����ƶ���
��3���������ʾ��ͼ��֪����ع���ʱ��ͨ�����������һ��Ϊȼ�ϵ�صĸ������������ⷽ��ʽ��֪��Ӧ�����������ӣ���Һ��pH���
�ڸ��ݵ�ʧ�����غ����ɵã�
��4��Na2HPO4�ĵ��볣����ˮ�ⳣ����С�ж�Na2HPO4��ˮ��Һ������ԡ�
��1������֪�Ȼ�ѧ����ʽ���α��Ϊ�٢ڢۣ��ɸ�˹���ɿ�֪���ڡ�2-��=�ۣ���K3=![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��2���������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�����ͼ��֪�����¶�����NO��ƽ��ת���ʼ�С��˵��ƽ�����淴Ӧ�����ƶ�������ӦΪ���ȷ�Ӧ����H��0���ʴ�Ϊ������
���ɷ�Ӧ�Ļ�ѧ����ʽ��֪���÷�Ӧ��ƽ�ⳣ������ʽkp=![]() ������ʼCO��NO�����ʵ���Ϊ1mol������������ɽ�����������ʽ��
������ʼCO��NO�����ʵ���Ϊ1mol������������ɽ�����������ʽ��
2CO(g)+2NO(g)![]() N2(g)+2CO2 (g)
N2(g)+2CO2 (g)
��mol�� 1 1 0 0
�䣨mol�� 0.7 0.7 0.35 0.7
ƽ��mol�� 0.3 0.3 0.35 0.7
������ʽ���ݿ�֪��ƽ��ʱ�����ʵ���Ϊ1.65mol��CO��NO��N2��CO2��ƽ���ѹ����Ϊ![]() ��1.65MPa��
��1.65MPa��![]() ��1.65MPa��
��1.65MPa��![]() ��1.65MPa��
��1.65MPa��![]() ��1.65Mpa����Ӧ��ƽ�ⳣ������ʽkp=
��1.65Mpa����Ӧ��ƽ�ⳣ������ʽkp=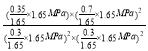 ��21.2��MPa��-1���ʴ�Ϊ��
��21.2��MPa��-1���ʴ�Ϊ��![]() ��21.2��MPa��-1��
��21.2��MPa��-1��
��NO�Ƿ�Ӧ�CO2��������淴Ӧ���У�NOŨ�ȼ�С��CO2Ũ����������ͼ��֪�������� v��
��3���������ʾ��ͼ��֪����ع���ʱ��ͨ�����������һ��Ϊȼ�ϵ�صĸ��������������ڸ���ʧ���ӷ���������Ӧ�����������������缫��ӦʽΪNO2+NO3--e-=N2O5���ɵ���������Һ������ӦΪCr2O72+6Fe2++14H+=2Cr3++6Fe3+ +7H2O��֪����Ӧ�����������ӣ���Һ��pH��ʴ�Ϊ��NO2+NO3--e-=N2O5�����
��ȼ�ϵ�ع���ʱ��1molO2��Ӧ��ת��4mol���ӣ����ݵ�ʧ�����غ��֪��4molNO2ת���N2O5��ת��4mol���ӣ���ͬ״�������������ȵ������ʵ���֮�ȣ���O2��NO2�������Ϊ1��4���ʴ�Ϊ��1��4��
��4��Na2HPO4��ˮ��Һ�з���ˮ�ⷴӦ��ˮ��ƽ��ΪHPO42��+H2O ![]() H2PO4��+OH����ˮ��ƽ�ⳣ��Kh2=
H2PO4��+OH����ˮ��ƽ�ⳣ��Kh2=![]() =
=![]() =
=![]() =1.6��10��7��Ka3=4.5��1013��HPO42-��ˮ��̶ȴ��ڵ���̶ȣ�����Һ�Լ��ԣ��ʴ�Ϊ���Na2HPO4��ˮ��ƽ�ⳣ��Kh2=
=1.6��10��7��Ka3=4.5��1013��HPO42-��ˮ��̶ȴ��ڵ���̶ȣ�����Һ�Լ��ԣ��ʴ�Ϊ���Na2HPO4��ˮ��ƽ�ⳣ��Kh2=![]() =
=![]() =
=![]() =1.6��10��7��Ka3=4.5��1013��HPO42-��ˮ��̶ȴ��ڵ���̶ȣ��ʶ��Լ��ԡ�
=1.6��10��7��Ka3=4.5��1013��HPO42-��ˮ��̶ȴ��ڵ���̶ȣ��ʶ��Լ��ԡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���ij���ݵ��ܱ������У�������ѧƽ�⣺C(s)+H2O(g)![]() CO(g)+H2(g)��������������˵���÷�Ӧ�Ѵﵽ��ѧƽ��״̬����
CO(g)+H2(g)��������������˵���÷�Ӧ�Ѵﵽ��ѧƽ��״̬����
A.��ϵ��ѹǿ���ٷ����仯B.v(CO)=v(H2O)
C.����nmolCO��ͬʱ����nmolH2D.1molH-H�����ѵ�ͬʱ�γ�2molH��O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��֤��ԭ��:SO2>Fe2+>C1-������ͬѧ�ֱ��������ͼʵ�飬������Һ1����Һ2���������ӽ����˼���,��֤��������ԭ��˳���ʵ������
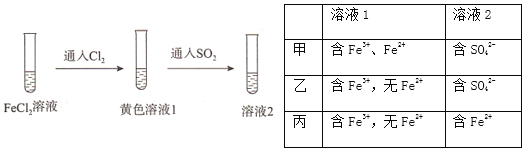
A. ֻ�м� B. �ס��� C. �ס��� D. �ס��ҡ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ú˴Ź������ⶨ�л�����ӵ���ά�ṹ���о������ŵ������ѧ�������л�������У���ͬλ�õ���ԭ�ӵĺ˴Ź��������и����ķ�ֵ(�ź�)Ҳ��ͬ�����ݷ�ֵ(�ź�)����ȷ���л����������ԭ�ӵ��������Ŀ��
���磺���ѵĽṹʽΪ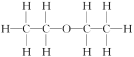 ����˴Ź�����������2����(�ź�)(�μ���ͼ)��
����˴Ź�����������2����(�ź�)(�μ���ͼ)��
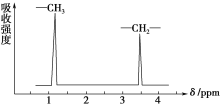
CH3CH2OCH2CH3�ĺ˴Ź�������
(1)���з����У���˴Ź���������ֻ��һ�ַ�(�ź�)��������________��
A��CH3CH3 B��CH3COOH C��CH3COOCH3 D��CH3COCH3
(2)������A��B�ķ���ʽ����C2H4Br��A�ĺ˴Ź���������ͼ��ʾ����A�Ľṹ��ʽΪ________����Ԥ��B�ĺ˴Ź�����������________����(�ź�)��
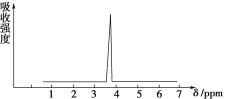
A�ĺ˴Ź�������ʾ��ͼ
(3)�ú˴Ź������ķ������о�C2H6O�Ľṹ�����Ҫ˵�����ݺ˴Ź������Ľ����ȷ��C2H6O���ӽṹ�ķ�����_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����������ͼװ�ô�����ʯȼ�Ͽ��ɡ��ӹ����̲�����H2S��������֪�����е������缫��Ϊ���Ե缫������˵������ȷ����
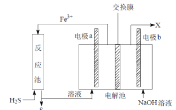
A.������ĤΪ���ӽ���Ĥ����NaOH��Һ��Ũ�������Ҫ���ڸ���
B.������ĤΪ�����ӽ���Ĥ��b �缫����������ɫ����
C.�缫 a Ϊ����
D.��Ӧ���д���H2S�ķ�Ӧ��H2S +2Fe3+ = 2Fe2+ +S��+2H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��G�������ʵ�ת����ϵ��ͼ��ʾ�����ַ�Ӧ�����ͷ�Ӧ����δ����������У�A��BΪ��ѧ��ѧ�����Ľ������ʣ�C�ǵ���ɫ���壬D������ǿ����Һ��Ӧ��������ǿ����Һ��Ӧ��F��Һ�м���AgNO3��Һ����������ϡ����İ�ɫ������E��G��ɫ��Ӧ���ʻ�ɫ���١��ܾ�Ϊȼ�շ�Ӧ��
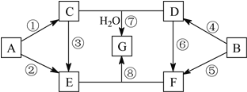
��ش��������⣺
(1)D�Ļ�ѧʽ____________��G�Ļ�ѧʽ____________��
(2)��Ҫ��д�����з�Ӧ�ķ���ʽ��
�۵Ļ�ѧ����ʽ��___________________��
B��E����Һ��Ӧ�����ӷ���ʽ��________________��
(3)��E����Һ��μ��뵽F����Һ������������������_____���ܷ�Ӧ�����ӷ���ʽΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ����ʽ����ȷ����
A.��Cl2��ʯ����ȡƯ��:2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O
B.��ҵ���ý�̼��ʯӢɰ�ƴֹ裺SiO2+C![]() Si+CO2
Si+CO2
C.����������ˮ������Ӧ��3Fe+4H2O![]() Fe3O4+4H2
Fe3O4+4H2
D.С�մ���Һ������ʯ��ˮ��Ӧ��2NaHCO3+Ca(OH)2=CaCO3��+Na2CO3+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���ϩ��(MTO)��ú��ϩ������·�ߵĺ��ļ�����ú��ϩ����Ҫ����ú��������Һ����ϩ���������Ρ�
��1��ú��Һ����������Ҫ��Ӧ֮һΪ2H2(g)+CO(g)��CH3OH (g) ��H��a kJ��mol1���ڲ�ͬ�¶��£�K(500��)��2.5 L2��mol2��K(700��)��0.2 L2��mol2��
�٦�H________0������������������������������
������Ӧ���ݻ�Ϊ2L���ܱ������н��У�500�����ijһʱ����ϵ��H2��CO��CH3OH���ʵ����ֱ�Ϊ2 mol��1 mol��3mol�����ʱ����CH3OH������____����CH3OH�����ʣ�����������������������������
��2��ͨ���о���������Է�Ӧ��Ӱ�죬��������״�������ϩ���ϩ�IJ��ʡ�
�״���ϩ������Ҫ��Ӧ�У�
i 2CH3OH(g)��C2H4(g)+2H2O(g) ��H1����20.9 kJ��mol1
ii3CH3OH(g)��C3H6(g)+3H2O(g) ��H2����98.1 kJ��mol1
iii 4CH3OH(g)��C4H8(g)+4H2O(g) ��H3����118.1 kJ��mol1
��C3H6ת��ΪC2H4���Ȼ�ѧ����ʽΪiv��2C3H6(g)![]() 3C2H4 (g) ��H4��____��
3C2H4 (g) ��H4��____��
������N2��Ϊϡ�ͼ�����Ӧi��C2H4�IJ��ʽ�_____������С�����䣩��
��3��Ϊ�о���ͬ�����Է�Ӧ��Ӱ�죬��ò�ͬ�¶���ƽ��ʱC2H4��C3H6��C4H8�����ʵ��������仯����ͼ��ʾ��
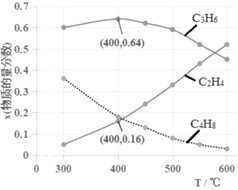
�������¶ȵ����ߣ�C3H6�����ʵ�������������������С�����ơ��¶ȸ���400��ʱ��ԭ����_____________________________�����¶ȵ���400��ʱ��ԭ����________________________��
����ϵ��ѹΪ0.1MPa��400��ʱ��Ӧiv��ƽ�ⳣ��Kp��________(��ʽ���㣬��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ�������)��
��Ϊ�˻�ø��ߵ�C2H4�ڲ����еı����������ƽϸ��¶ȵ������⣬���½����˵���______��
A������ˮ���� B������ˮ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ��������У����и�������һ�������������
A. ���ȳʺ�ɫ����Һ�У�K+��Na+��S2����AlO2��
B. ![]() =1��10��13mol��L��1����Һ�У�NH4����Ca2����Cl����NO3��
=1��10��13mol��L��1����Һ�У�NH4����Ca2����Cl����NO3��
C. �����£���![]() = 1��1012����Һ�У�NH4+��CO32����K+��Cl��
= 1��1012����Һ�У�NH4+��CO32����K+��Cl��
D. �����£�ˮ�������c(OH��)=1��10��13 mol/L����Һ�У�Na+��NH4+��HCO3����NO3��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com