
”¾ĢāÄæ”æ·°¾ßÓŠ¹ć·ŗÓĆĶ¾”£š¤ĶĮ·°æóÖŠ£¬·°ŅŌ+3”¢+4”¢+5¼ŪµÄ»ÆŗĻĪļ“ęŌŚ£¬»¹°üĄØ¼Ų”¢Ć¾µÄĀĮ¹čĖįŃĪ£¬ŅŌ¼°SiO2”¢Fe3O4”£²ÉÓĆŅŌĻĀ¹¤ŅÕĮ÷³ĢæÉÓÉš¤ĶĮ·°æóÖʱøNH4VO3”£
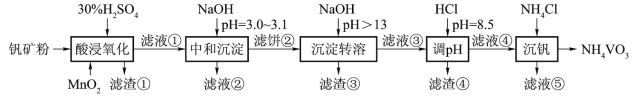
øĆ¹¤ŅÕĢõ¼žĻĀ£¬ČÜŅŗÖŠ½šŹōĄė×ÓæŖŹ¼³ĮµķŗĶĶźČ«³ĮµķµÄpHČēĻĀ±ķĖłŹ¾£ŗ
½šŹōĄė×Ó | Fe3+ | Fe2+ | Al3+ | Mn2+ |
æŖŹ¼³ĮµķpH | 1.9 | 7.0 | 3.0 | 8.1 |
ĶźČ«³ĮµķpH | 3.2 | 9.0 | 4.7 | 10.1 |
»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)”°Ėį½žŃõ»Æ”±ŠčŅŖ¼ÓČČ£¬ĘäŌŅņŹĒ___________”£
(2)”°Ėį½žŃõ»Æ”±ÖŠ£¬VO+ŗĶVO2+±»Ńõ»Æ³É![]() £¬Ķ¬Ź±»¹ÓŠ___________Ąė×Ó±»Ńõ»Æ”£Š“³öVO+×Ŗ»ÆĪŖ
£¬Ķ¬Ź±»¹ÓŠ___________Ąė×Ó±»Ńõ»Æ”£Š“³öVO+×Ŗ»ÆĪŖ![]() ·“Ó¦µÄĄė×Ó·½³ĢŹ½___________”£
·“Ó¦µÄĄė×Ó·½³ĢŹ½___________”£
(3)”°ÖŠŗĶ³Įµķ”±ÖŠ£¬·°Ė®½ā²¢³ĮµķĪŖ![]() £¬ĖęĀĖŅŗ¢ŚæɳżČ„½šŹōĄė×ÓK+”¢Mg2+”¢Na+”¢___________£¬ŅŌ¼°²æ·ÖµÄ___________”£
£¬ĖęĀĖŅŗ¢ŚæɳżČ„½šŹōĄė×ÓK+”¢Mg2+”¢Na+”¢___________£¬ŅŌ¼°²æ·ÖµÄ___________”£
(4)”°³Įµķ×ŖČÜ”±ÖŠ£¬![]() ×Ŗ»ÆĪŖ·°ĖįŃĪČܽā”£ĀĖŌü¢ŪµÄÖ÷ŅŖ³É·ÖŹĒ___________”£
×Ŗ»ÆĪŖ·°ĖįŃĪČܽā”£ĀĖŌü¢ŪµÄÖ÷ŅŖ³É·ÖŹĒ___________”£
(5)”°µ÷pH”±ÖŠÓŠ³ĮµķÉś²ś£¬Éś³É³Įµķ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ___________”£
(6)”°³Į·°”±ÖŠĪö³öNH4VO3¾§ĢåŹ±£¬ŠčŅŖ¼ÓČė¹żĮæNH4Cl£¬ĘäŌŅņŹĒ___________”£
”¾“š°ø”æ¼ÓæģĖį½žŗĶŃõ»Æ·“Ó¦ĖŁĀŹ£Ø“Ł½ųŃõ»ÆĶźČ«£© Fe2+ VO++MnO2+2H+=![]() +Mn2++H2O Mn2+ Fe3+”¢Al3+ Fe(OH)3 NaAlO2+HCl+H2O=NaCl+Al(OH)3”ż»ņNa[Al(OH)4]+HCl= NaCl+Al(OH)3”ż+H2O ĄūÓĆĶ¬Ąė×ÓŠ§Ó¦£¬“Ł½ųNH4VO3¾”æÉÄÜĪö³öĶźČ«
+Mn2++H2O Mn2+ Fe3+”¢Al3+ Fe(OH)3 NaAlO2+HCl+H2O=NaCl+Al(OH)3”ż»ņNa[Al(OH)4]+HCl= NaCl+Al(OH)3”ż+H2O ĄūÓĆĶ¬Ąė×ÓŠ§Ó¦£¬“Ł½ųNH4VO3¾”æÉÄÜĪö³öĶźČ«
”¾½āĪö”æ
š¤ĶĮ·°æóÖŠ£¬·°ŅŌ+3”¢+4”¢+5¼ŪµÄ»ÆŗĻĪļ“ęŌŚ£¬»¹°üĄØ¼Ų”¢Ć¾µÄĀĮ¹čĖįŃĪ£¬ŅŌ¼°SiO2”¢Fe3O4£¬ÓĆ30%H2SO4ŗĶMnO2”°Ėį½žŃõ»Æ”±Ź±VO+ŗĶVO2+±»Ńõ»Æ³É![]() £¬Fe3O4ÓėĮņĖį·“Ӧɜ³ÉµÄFe2+±»Ńõ»Æ³ÉFe3+£¬SiO2“Ė¹ż³ĢÖŠ²»·“Ó¦£¬ĀĖŅŗ¢ŁÖŠŗ¬ÓŠ
£¬Fe3O4ÓėĮņĖį·“Ӧɜ³ÉµÄFe2+±»Ńõ»Æ³ÉFe3+£¬SiO2“Ė¹ż³ĢÖŠ²»·“Ó¦£¬ĀĖŅŗ¢ŁÖŠŗ¬ÓŠ![]() ”¢K+”¢Mg2+”¢Al3+”¢Fe3+”¢Mn2+”¢
”¢K+”¢Mg2+”¢Al3+”¢Fe3+”¢Mn2+”¢![]() £»ĀĖŅŗ¢ŁÖŠ¼ÓČėNaOHµ÷½ŚpH=3.0~3.1£¬·°Ė®½ā²¢³ĮµķĪŖV2O5”¤xH2O£¬øł¾Ż±ķÖŠĢį¹©µÄČÜŅŗÖŠ½šŹōĄė×ÓæŖŹ¼³ĮµķŗĶĶźČ«³ĮµķµÄpH£¬“Ė¹ż³ĢÖŠFe3+²æ·Ö×Ŗ»ÆĪŖFe(OH)3³Įµķ£¬²æ·ÖAl3+×Ŗ»ÆĪŖAl(OH)3³Įµķ£¬ĀĖŅŗ¢ŚÖŠŗ¬ÓŠK+”¢Na+”¢Mg2+”¢Al3+”¢Fe3+”¢Mn2+”¢
£»ĀĖŅŗ¢ŁÖŠ¼ÓČėNaOHµ÷½ŚpH=3.0~3.1£¬·°Ė®½ā²¢³ĮµķĪŖV2O5”¤xH2O£¬øł¾Ż±ķÖŠĢį¹©µÄČÜŅŗÖŠ½šŹōĄė×ÓæŖŹ¼³ĮµķŗĶĶźČ«³ĮµķµÄpH£¬“Ė¹ż³ĢÖŠFe3+²æ·Ö×Ŗ»ÆĪŖFe(OH)3³Įµķ£¬²æ·ÖAl3+×Ŗ»ÆĪŖAl(OH)3³Įµķ£¬ĀĖŅŗ¢ŚÖŠŗ¬ÓŠK+”¢Na+”¢Mg2+”¢Al3+”¢Fe3+”¢Mn2+”¢![]() £¬ĀĖ±ż¢ŚÖŠŗ¬V2O5”¤xH2O”¢Fe(OH)3”¢Al(OH)3£¬ĀĖ±ż¢ŚÖŠ¼ÓČėNaOHŹ¹pH>13£¬V2O5”¤xH2O×Ŗ»ÆĪŖ·°ĖįŃĪČܽā£¬Al(OH)3×Ŗ»ÆĪŖNaAlO2£¬ŌņĀĖŌü¢ŪµÄÖ÷ŅŖ³É·ÖĪŖFe(OH)3£»ĀĖŅŗ¢ŪÖŠŗ¬·°ĖįŃĪ”¢Ę«ĀĮĖįÄĘ£¬¼ÓČėHClµ÷pH=8.5£¬NaAlO2×Ŗ»ÆĪŖAl(OH)3³Įµķ¶ų³żČ„£»×īŗóĻņĀĖŅŗ¢ÜÖŠ¼ÓČėNH4Cl”°³Į·°”±µĆµ½NH4VO3”£
£¬ĀĖ±ż¢ŚÖŠŗ¬V2O5”¤xH2O”¢Fe(OH)3”¢Al(OH)3£¬ĀĖ±ż¢ŚÖŠ¼ÓČėNaOHŹ¹pH>13£¬V2O5”¤xH2O×Ŗ»ÆĪŖ·°ĖįŃĪČܽā£¬Al(OH)3×Ŗ»ÆĪŖNaAlO2£¬ŌņĀĖŌü¢ŪµÄÖ÷ŅŖ³É·ÖĪŖFe(OH)3£»ĀĖŅŗ¢ŪÖŠŗ¬·°ĖįŃĪ”¢Ę«ĀĮĖįÄĘ£¬¼ÓČėHClµ÷pH=8.5£¬NaAlO2×Ŗ»ÆĪŖAl(OH)3³Įµķ¶ų³żČ„£»×īŗóĻņĀĖŅŗ¢ÜÖŠ¼ÓČėNH4Cl”°³Į·°”±µĆµ½NH4VO3”£
(1)”°Ėį½žŃõ»Æ”±ŠčŅŖ¼ÓČČ£¬ĘäŌŅņŹĒ£ŗÉżøßĪĀ¶Č£¬¼ÓæģĖį½žŗĶŃõ»Æ·“Ó¦ĖŁĀŹ£Ø“Ł½ųŃõ»ÆĶźČ«£©£¬¹Ź“š°øĪŖ£ŗ¼ÓæģĖį½žŗĶŃõ»Æ·“Ó¦ĖŁĀŹ£Ø“Ł½ųŃõ»ÆĶźČ«£©£»
(2)”°Ėį½žŃõ»Æ”±ÖŠ£¬·°æó·ŪÖŠµÄFe3O4ÓėĮņĖį·“Ӧɜ³ÉFeSO4”¢Fe2(SO4)3ŗĶĖ®£¬MnO2¾ßÓŠŃõ»ÆŠŌ£¬Fe2+¾ßÓŠ»¹ŌŠŌ£¬ŌņVO+ŗĶVO2+±»Ńõ»Æ³É![]() µÄĶ¬Ź±»¹ÓŠFe2+±»Ńõ»Æ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖMnO2+2Fe2++4H+=Mn2++2Fe3++2H2O£»VO+×Ŗ»ÆĪŖ
µÄĶ¬Ź±»¹ÓŠFe2+±»Ńõ»Æ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖMnO2+2Fe2++4H+=Mn2++2Fe3++2H2O£»VO+×Ŗ»ÆĪŖ![]() Ź±£¬·°ŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+3¼ŪÉżÖĮ+5¼Ū£¬1molVO+Ź§Č„2molµē×Ó£¬MnO2±»»¹ŌĪŖMn2+£¬MnŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+4¼Ū½µÖĮ+2¼Ū£¬1molMnO2µĆµ½2molµē×Ó£¬øł¾ŻµĆŹ§µē×ÓŹŲŗć”¢Ō×ÓŹŲŗćŗĶµēŗÉŹŲŗć£¬VO+×Ŗ»ÆĪŖ
Ź±£¬·°ŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+3¼ŪÉżÖĮ+5¼Ū£¬1molVO+Ź§Č„2molµē×Ó£¬MnO2±»»¹ŌĪŖMn2+£¬MnŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+4¼Ū½µÖĮ+2¼Ū£¬1molMnO2µĆµ½2molµē×Ó£¬øł¾ŻµĆŹ§µē×ÓŹŲŗć”¢Ō×ÓŹŲŗćŗĶµēŗÉŹŲŗć£¬VO+×Ŗ»ÆĪŖ![]() ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖVO++MnO2+2H+=
·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖVO++MnO2+2H+=![]() +Mn2++H2O£¬¹Ź“š°øĪŖ£ŗFe2+£¬VO++MnO2+2H+=
+Mn2++H2O£¬¹Ź“š°øĪŖ£ŗFe2+£¬VO++MnO2+2H+=![]() +Mn2++H2O£»
+Mn2++H2O£»
(3)øł¾Ż·ÖĪö£¬”°ÖŠŗĶ³Įµķ”±ÖŠ£¬·°Ė®½ā²¢³ĮµķĪŖV2O5”¤xH2O£¬ĖęĀĖŅŗ¢ŚæɳżČ„½šŹōĄė×ÓK+”¢Mg2+”¢Na+”¢Mn2+£¬ŅŌ¼°²æ·ÖµÄFe3+”¢Al3+£¬¹Ź“š°øĪŖ£ŗMn2+£¬Fe3+”¢Al3+£»
(4)øł¾Ż·ÖĪö£¬ĀĖŌü¢ŪµÄÖ÷ŅŖ³É·ÖŹĒFe(OH)3£¬¹Ź“š°øĪŖ£ŗFe(OH)3£»
(5)”°µ÷pH”±ÖŠÓŠ³ĮµķÉś³É£¬ŹĒNaAlO2ÓėHCl·“Ӧɜ³ÉAl(OH)3³Įµķ£¬Éś³É³Įµķ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒNaAlO2+HCl+H2O=NaCl+Al(OH)3”ż»ņNa[Al(OH)4]+HCl= NaCl+Al(OH)3”ż+H2O£¬¹Ź“š°øĪŖ£ŗNaAlO2+HCl+H2O=NaCl+Al(OH)3”ż»ņNa[Al(OH)4]+HCl= NaCl+Al(OH)3”ż+H2O”£
(6)”°³Į·°”±ÖŠĪö³öNH4VO3¾§ĢåŹ±£¬ŠčŅŖ¼ÓČė¹żĮæNH4Cl£¬ĘäŌŅņŹĒ£ŗŌö“óNH4+Ąė×ÓÅØ¶Č£¬ĄūÓĆĶ¬Ąė×ÓŠ§Ó¦£¬“Ł½ųNH4VO3¾”æÉÄÜĪö³öĶźČ«£¬¹Ź“š°øĪŖ£ŗĄūÓĆĶ¬Ąė×ÓŠ§Ó¦£¬“Ł½ųNH4VO3¾”æÉÄÜĪö³öĶźČ«”£


 ½šÅĘ½ĢøØÅąÓÅÓÅŃ”¾ķĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
½šÅĘ½ĢøØÅąÓÅÓÅŃ”¾ķĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖ²ā¶Ø![]() ѳʷµÄ“æ¶Č£¬ÓĆĮņĖįČܽā6.300 gѳʷ£¬¶ØČŻÖĮ250 mL”£Č”25.00 mLČÜŅŗ£¬ÓĆ
ѳʷµÄ“æ¶Č£¬ÓĆĮņĖįČܽā6.300 gѳʷ£¬¶ØČŻÖĮ250 mL”£Č”25.00 mLČÜŅŗ£¬ÓĆ![]() ±ź×¼ČÜŅŗµĪ¶ØÖĮÖÕµć”£ÖŲø“ŹµŃ飬Źż¾ŻČēĻĀ£ŗ
±ź×¼ČÜŅŗµĪ¶ØÖĮÖÕµć”£ÖŲø“ŹµŃ飬Źż¾ŻČēĻĀ£ŗ
ŠņŗÅ | µĪ¶ØĒ°¶ĮŹż/mL | µĪ¶ØÖÕµć¶ĮŹż/mL |
1 | 0.00 | 19.98 |
2 | 1.26 | 22.40 |
3 | 1.54 | 21.56 |
ŅŃÖŖ£ŗ![]()
¼ŁÉčŌÓÖŹ²»²Ī¼Ó·“Ó¦”£
øĆѳʷ֊![]() µÄÖŹĮæ·ÖŹżŹĒ________%£Ø±£ĮōŠ”ŹżµćŗóŅ»Ī»£©£»
µÄÖŹĮæ·ÖŹżŹĒ________%£Ø±£ĮōŠ”ŹżµćŗóŅ»Ī»£©£»
Š“³ö¼ņŅŖ¼ĘĖć¹ż³Ģ£ŗ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫agijĪļÖŹŌŚ×ćĮæŃõĘųÖŠ³ä·ÖČ¼ÉÕŌŁ½«ĘųĢåÉś³ÉĪļĶØČė×ćĮæµÄNa2O2³ä·Ö·“Ó¦£¬¹ĢĢåŌöÖŲĪŖbg£¬Čōa<b£¬ŌņøĆĪļÖŹæÉÄÜŹĒ£Ø £©
A. H2B. COC. ŅŅĖį(CH3COOH)D. ¼×Ķé(CH4)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉĻ±½ŅŅĻ©ŹĒŗĻ³ÉŹ÷Ö¬”¢Ąė×Ó½»»»Ź÷Ö¬¼°ŗĻ³ÉĻš½ŗµČµÄÖŲŅŖµ„Ģ壬ČēĶ¼ŹĒ±½ŅŅĻ©µÄ½į¹¹¼ņŹ½£ŗ![]() ,ĻĀĮŠ¹ŲÓŚøĆÓŠ»śĪļµÄĖµ·Ø²»ÕżČ·µÄŹĒ(””””)
,ĻĀĮŠ¹ŲÓŚøĆÓŠ»śĪļµÄĖµ·Ø²»ÕżČ·µÄŹĒ(””””)
A. ±½ŅŅĻ©µÄ·Ö×ÓŹ½ĪŖC8H8
B. ±½ŅŅĻ©Ķعż¼Ó¾Ū·“Ó¦æÉÖʱøøß·Ö×Ó»ÆŗĻĪļ
C. ±½ŅŅĻ©ÓėäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗ·“Ó¦£ŗ![]()
D. ±½ŅŅĻ©ÄÜ·¢Éś¼Ó³É·“Ó¦£¬µ«²»ÄÜ·¢ÉśČ”“ś·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉĻĶس£ĄūÓĆSiO2 ŗĶĢ¼·“Ó¦Ą“ÖĘČ”¹č£¬Š“³ö·“Ó¦µÄ»Æѧ·½³ĢŹ½___________________”£
¹¤ŅµÉĻ»¹æÉŅŌĄūÓĆĆ¾ÖĘČ”¹č£¬·“Ó¦ĪŖ2Mg+SiO2 = 2MgO+Si£¬Ķ¬Ź±»į·¢Éśø±·“Ó¦£ŗ2Mg + Si = Mg2Si”£ČēĶ¼ŹĒ½ųŠŠMgÓėSiO2·“Ó¦µÄŹµŃé×°ÖĆ£¬ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ

£Ø1£©ÓÉÓŚO2ŗĶH2O£Øg£©µÄ“ęŌŚ¶ŌøĆŹµŃéÓŠ½Ļ“óÓ°Ļģ£¬ŹµŃéÖŠÓ¦ĶØČėĘųĢåX×÷ĪŖ±£»¤Ęų£¬ŹŌ¹ÜÖŠµÄ¹ĢĢåŅ©Ę·æÉŃ”ÓĆ________(ĢīŠņŗÅ)”£
a£®ŹÆ»ŅŹÆ””””””b£®ŠæĮ£””””””c£®“æ¼ī
£Ø2£©ŹµŃéæŖŹ¼Ź±£¬±ŲŠėĻČĶØŅ»¶ĪŹ±¼äXĘųĢ壬ŌŁ¼ÓČČ·“Ó¦Īļ£¬ĘäĄķÓÉŹĒ ___________________________£»µ±·“Ó¦Ņż·¢ŗó£¬ŅĘ×ß¾Ę¾«µĘ£¬·“Ó¦ÄܼĢŠų½ųŠŠ£¬ĘäŌŅņŹĒ______________________”£
£Ø3£©·“Ó¦½įŹųŗ󣬓żĄäČ“ÖĮ³£ĪĀŹ±£¬Ķł·“Ó¦ŗóµÄ»ģŗĻĪļÖŠ¼ÓČėĻ”ŃĪĖį£¬æɹŪ²ģµ½ÉĮĮĮµÄ»šŠĒ£¬²śÉś“ĖĻÖĻóµÄŌŅņŹĒø±²śĪļMg2SiÓöŃĪĖįŃøĖŁ·“Ӧɜ³ÉSiH4£Ø¹čĶ飩ĘųĢå£¬Č»ŗóSiH4×ŌČ¼£®ÓĆ»Æѧ·½³ĢŹ½±ķŹ¾ÕāĮ½øö·“Ó¦¢Ł________________________¢Ś___________________£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚČČ»Æѧ·“Ó¦µÄĆčŹöÖŠÕżČ·µÄŹĒ( )
A.HClÓėNaOH·“Ó¦µÄÖŠŗĶČČ”÷H£½£57.3kJ/mol£¬ŌņH2SO4ŗĶ°±Ė®·“Ó¦µÄÖŠŗĶČČ”÷H£½2”Į(£57.3)kJ/mol
B.CO(g)µÄČ¼ÉÕČČŹĒ283.0kJ/mol£¬Ōņ2CO2(g)£½2CO(g)£«O2(g)µÄ·“Ó¦ČČ”÷H£½£«566.0kJ/mol
C.ŠčŅŖ¼ÓČČ²ÅÄÜ·¢ÉśµÄ·“Ó¦Ņ»¶ØŹĒĪüČČ·“Ó¦
D.1mol¼×ĶéČ¼ÉÕÉś³ÉĘųĢ¬Ė®ŗĶ¶žŃõ»ÆĢ¼Ėł·Å³öµÄČČĮæŹĒ¼×ĶéµÄČ¼ÉÕČČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖH2(g)£«I2(g)![]() 2HI(g)¦¤H<0”£ÓŠĻąĶ¬ČŻ»żµÄ¶ØČŻĆܱÕČŻĘ÷¼×ŗĶŅŅ£¬¼×ÖŠ¼ÓČėH2ŗĶI2ø÷0.1mol£¬ŅŅÖŠ¼ÓČėHI0.2mol£¬ŌŚĻąĶ¬ĪĀ¶ČĻĀ·Ö±š“ļµ½Ę½ŗā”£ĻÖÓūŹ¹¼×ÖŠHIĘ½ŗāŹ±µÄ°Ł·Öŗ¬Įæ“óÓŚŅŅÖŠHIĘ½ŗāŹ±µÄ°Ł·Öŗ¬Į棬ŌņÓ¦²ÉČ”µÄ“ėŹ©ŹĒ
2HI(g)¦¤H<0”£ÓŠĻąĶ¬ČŻ»żµÄ¶ØČŻĆܱÕČŻĘ÷¼×ŗĶŅŅ£¬¼×ÖŠ¼ÓČėH2ŗĶI2ø÷0.1mol£¬ŅŅÖŠ¼ÓČėHI0.2mol£¬ŌŚĻąĶ¬ĪĀ¶ČĻĀ·Ö±š“ļµ½Ę½ŗā”£ĻÖÓūŹ¹¼×ÖŠHIĘ½ŗāŹ±µÄ°Ł·Öŗ¬Įæ“óÓŚŅŅÖŠHIĘ½ŗāŹ±µÄ°Ł·Öŗ¬Į棬ŌņÓ¦²ÉČ”µÄ“ėŹ©ŹĒ
A. ¼×”¢ŅŅĢįøßĻąĶ¬ĪĀ¶Č B. ¼×ÖŠ¼ÓČė0.1molHe£¬ŅŅÖŠ²»±ä
C. ¼×½µµĶĪĀ¶Č£¬ŅŅŌö“óŃ¹Ēæ D. ¼×Ōö¼Ó0.1molH2£¬ŅŅŌö¼Ó0.1molI2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢ½¾æŠĀÖʱ„ŗĶĀČĖ®³É·ÖµÄŹµŃéÖŠ£¬ĻĀĮŠøł¾ŻŹµŃéĻÖĻóµĆ³öµÄ½įĀŪÕżČ·µÄŹĒ
A.ŠĀÖʱ„ŗĶĀČĖ®Ź¹ŗģƵ¹å±äĮ¦°×Ƶ¹å£¬ĖµĆ÷ŗ¬ÓŠCl2
B.¼ÓČėŹÆČļČÜŅŗ£¬ČÜŅŗ±äŗģ£¬ĖµĆ÷øĆČÜŅŗ²»ŗ¬HC1O
C.¹āÕÕŠĀÖĘĀČĖ®ÓŠĘųÅŻŅŻ³ö£¬øĆĘųĢåŹĒŃõĘų
D.ĻņĀČĖ®ÖŠKHCO3·ŪÄ©ÓŠĘųÅŻ²śÉś£¬ĖµĆ÷ĀĢĖ®ÖŠŗ¬ÓŠHC1O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
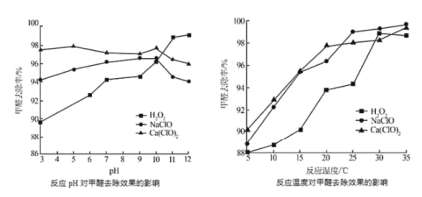
”¾ĢāÄæ”æ¼×Č©(HCHO)ŌŚ»Æ¹¤”¢Ņ½Ņ©”¢Å©Ņ©µČµÄ·½ĆęÓŠ¹ć·ŗÓ¦ÓĆ”£
(1)¼×“¼ĶŃĒā·ØæÉÖʱø¼×Č©(·“Ó¦ĢåĻµÖŠø÷ĪļÖŹ¾łĪŖĘųĢ¬)£¬½įŗĻČēĶ¼Ķ¼Ļń»Ų“šĪŹĢā”£
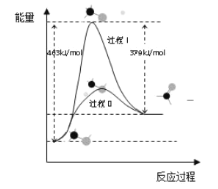
¢Ł“Ė·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ŹĒ______”£
¢Ś·“Ó¦»ī»ÆÄÜ£ŗ¹ż³ĢI______¹ż³ĢII (Ģī”°>”±”°=”±»ņ”°<”±)
¢Ū¹ż³ĢIIĪĀ¶Č”Ŗ×Ŗ»ÆĀŹĶ¼ČēĶ¼£¬ĻĀĮŠĖµ·ØŗĻĄķµÄŹĒ_____”£
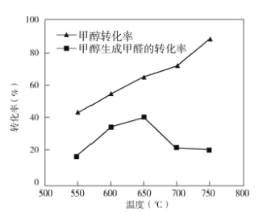
A.¼×“¼ĶŃĒā·ØÖʱø¼×Č©¹ż³ĢĪŽø±·“Ó¦·¢Éś
B.ĪĀ¶ČøßÓŚ650”ćC“߻ƼĮÉÕ½į£¬»īŠŌ¼õČõ
C.¼°Ź±·ÖĄė²śĘ·ÓŠĄūÓŚĢįø߼ד¼Éś³É¼×Č©µÄ×Ŗ»ÆĀŹ
(2)¼×Č©³¬±ź»įĪ£ŗ¦ČĖĢ彔浣¬Šč¶Ō¼×Č©ĶłŠŠŗ¬Įæ¼ģ²ā¼°ĪŪČ¾“¦Ąķ”£
¢ŁÄ³¼×Č©ĘųĢå“«øŠĘ÷µÄ¹¤×÷ŌĄķČēĶ¼ĖłŹ¾£¬b¼«µÄµē¼«·“Ó¦Ź½ĪŖ_________
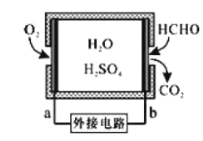
¢ŚŃõ»Æ¼ĮæÉ“¦Ąķ¼×Č©ĪŪČ¾£¬½įŗĻŅŌČēĶ¼Ķ¼Ļń·ÖĪö“ŗ¼¾(Ė®ĪĀŌ¼15”ę)Ó¦¼±“¦Ąķ¼×Č©ĪŪČ¾µÄĖ®Ō“ӦєŌńµÄŹŌ¼ĮĪŖ________”£
(3)750KĻĀ£¬ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ£¬³äČėµÄ¼×“¼£¬·¢Éś·“Ó¦£ŗCH3OH(g)HCHO(g) + H2(g)£¬ČōĘšŹ¼Ń¹ĒæĪŖ101kPa£¬ “ļµ½Ę½ŗā×Ŗ»ÆĀŹĪŖ50.0%£¬ Ōņ·“Ó¦Ę½ŗāµÄ³£ŹżKp= ______”£(ÓĆĘ½ŗā·ÖŃ¹“śĢęĘ½ŗāÅ©¶Č¼ĘĖć£¬·ÖŃ¹£½×ÜŃ¹”ĮĪļÖŹµÄĮæ·ÖŹż£¬ŗöĀŌĘäĖü·“Ó¦)”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com