
【题目】以海水为电解质的Mg-AgCl电池在军事上可用作电动鱼雷的电源,其电池反应离子方程式为:2AgCl+Mg=Mg2++2Ag+2Cl-。该电池工作时,下列说法正确的是

A. 正、负极的质量均减少 B. AgCl电极发生氧化反应
C. 电子由AgCl经外电路流向Mg D. 实现了电能向化学能的转化
科目:高中化学 来源: 题型:
【题目】甲烷是一种重要的化工原料和清洁能源,研究其再生及合理利用有重要意义。
请回答:
(1)已知一定条件下发生如下反应:
CO2(g)+2H2O(g)![]() CH4(g)+2O2(g) △H=+802kJ·mol-1。
CH4(g)+2O2(g) △H=+802kJ·mol-1。
将一定量的CO2(g)和H2O(g)充入10L密闭容器中,分别在催化剂M、N的作用下发生上述反应,CH4(g)的产量(n)与光照时间(t)和温度(T)变化的关系如图1所示。
①若甲烷的燃烧热(△H)为-890kJ·mol-1,则水的汽化热△H=___________。(汽化热指1mol液体转化为气体时吸收的热量)
②T1℃、催化剂M作用下,0~20h内该反应速率v(H2O)=___________。

③根据图1判断,T1___________T2(填“>”“<”或“=”),理由为___________。
催化剂的催化效果:M___________N(填“强于”或“弱于”)。
(2)甲烷可用于制备合成气:CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H。将CH4(g)和H2O(g)以物质的量之比为1:3充入盛有催化剂的刚性容器中发生该反应。相同时间段内测得CO的体积分数(
CO(g)+3H2(g) △H。将CH4(g)和H2O(g)以物质的量之比为1:3充入盛有催化剂的刚性容器中发生该反应。相同时间段内测得CO的体积分数(![]() )与温度(T)的关系如图2所示。
)与温度(T)的关系如图2所示。
①T0℃时,CO的体积分数最大的原因为_________________________________。
②若T0℃时,容器内起始压强为p0,CO的平衡体积分数为10%,则反应的平衡常数Kp=___________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨烯锂硫电池电解制备Fe(OH)2的装置如图所示。电池放电时的反应为16Li+xS8==8Li2Sx(2≤x≤8),电解池两极材料分别为Fe和石墨,工作一段时间后,右侧玻璃管中产生大量的白色沉淀。下列说法不正确的是
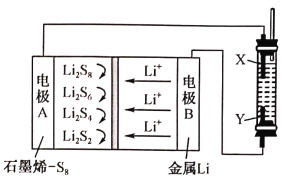
A. X是铁电极,发生氧化反应
B. 电子流动的方向:B→Y,X→A
C. 正极可发生反应:2Li2S6+2Li++2e-=3Li2S4
D. 锂电极减重0.14g时,电解池中溶液减重0.18g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙烯和聚乙烯的叙述不正确的是( )
A. 乙烯常温下是气体,为纯净物;聚乙烯常温下是固体,为混合物
B. 乙烯的化学性质比聚乙烯活泼
C. 取等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等
D. 乙烯和聚乙烯都能使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,它们的原子最外层电子数总和等于Z的原子序数,由这四种元素组成一种化合物M具有如下性质下列推断正确的是

A. 原子半径:Z>Y>X>W
B. 最高价氧化物对应的水化物酸性:Y>X
C. 简单阴离子的还原性:W<Z
D. W、Y、Z组成的化合物只含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是( )

A. 图甲表示1 mL pH=2某一元酸溶液加水稀释时,pH随溶液总体积的变化曲线,说明该酸是强酸
B. 图乙表示恒容密闭容器中其他条件相同时改变温度,反应CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ
CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ
C. 图丙表示不同温度下水溶液中-lg c(H+)、-lg c(OH-)变化曲线,说明T1>T2
D. 图丁表示1 mol H2和0.5 mol O2反应生成1 mol H2O过程中的能量变化曲线,说明H2的燃烧热是241.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】⑴根据分子中所含官能团可预测有机化合物的性质。
①下列化合物中,能与H2发生加成反应的是______(填字母)。
a.CH3Cl b.CH2=CH2 c.CH3CH2OH
②下列化合物中,能发生水解反应的是______(填字母)。
a.蔗糖 b.乙酸 c.乙醇
③下列有机物中易溶于水的是______(填字母)。
a.乙烯 b.乙酸乙酯 c.葡萄糖
⑵苯甲醇(![]() )是一重要的有机化工原料,在一定条件下可发生如下反应:
)是一重要的有机化工原料,在一定条件下可发生如下反应:
2![]() +O2
+O2![]() 2
2![]() +2H2O
+2H2O
①苯甲醇的分子式为______。
②苯甲醇中所含官能团的名称是______,![]() 中所含官能团的名称是______。
中所含官能团的名称是______。
③苯甲醇性质与乙醇相似,下列物质中不能与苯甲醇反应的是______(填字母)。
a.NaOH b.Na c.乙酸
④该反应的反应类型是______(填字母)。
a.加成反应 b.氧化反应 c.酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铂钴合金是以铂为基含钴二元合金,在高温下,铂与钴可无限互溶,其固溶体为面心立方晶格。铂钴合金磁性极强,磁稳定性较高,耐化学腐蚀性很好,主要用于航天航空仪表、电子钟表、磁控管等。
(1)基态钴原子的价电子排布图为___________。
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体(如下图)。科学研究表明,顺式分子具有抗癌活性。

①吡啶分子是大体积平面配体,其结构简式如图所示![]() 。每个吡啶分子中含有的σ键数目为___________。吡啶分子中所含的各元素的电负性由大到小的顺序是___________。
。每个吡啶分子中含有的σ键数目为___________。吡啶分子中所含的各元素的电负性由大到小的顺序是___________。
②二氯二吡啶合铂中存在的微粒间作用力有___________(填字母)。
a.范德华力 b.氢键 c.金属键 d.非极性键
③反式二氯二吡啶合铂分子是___________(填“极性分子”或“非极性分子”)。

(3)某研究小组将平面型的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如下图所示。
①“分子金属”可以导电,是因为___________能沿着其中的金属原子链流动。
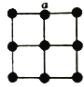
②“分子金属”中,铂原子是否以sp3的方式杂化?_________(填“是”或“否”),其理由是_______。
(4)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y或z轴的投影图如图所示。若金属铂的密度为dg·cm-3,则晶胞参数a=______nm(列计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验(夹持装置未画出),能达到实验目的的是
A. 实验甲:CuSO4溶液中会形成一条光亮的通路
B. 实验乙:试管中溶液变为红色
C. 实验丙:将湿润的有色布条放入盛有干燥氯气的瓶中,布条不褪色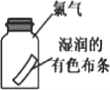
D. 实验丁:将灼烧至黑色的铜丝插入无水乙醇,铜丝变成紫红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com