
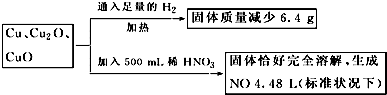
| A、4.4 mol?L-1 |
| B、3.6 mol?L-1 |
| C、4.0 mol?L-1 |
| D、3.2 mol?L-1 |
|


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
| A、石墨的层状结构中由共价键形成的最小的碳原子环上有六个碳原子 |
| B、氯化钠晶体中每个Na+或Cl-周围紧邻的有6个Cl-或Na+ |
| C、在CsCl晶体中每个Cs+周围紧邻的有8个Cl-,而和每个Cs+等距离紧邻的也有8个Cs+ |
| D、在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有4个金属原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3═Na++H++CO32- |
| B、Ba(OH)2═Ba2++OH- |
| C、Al2(SO4)3═2Al3++3SO42- |
| D、H2SO4═H2++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、⑤⑥ |
| C、②③⑥ | D、③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 乙酸乙酯是一种用途广泛的精细化工产品.某课外小组设计实验室制取并提纯乙酸乙酯的方案如下:
乙酸乙酯是一种用途广泛的精细化工产品.某课外小组设计实验室制取并提纯乙酸乙酯的方案如下:| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
| 浓硫酸 |
| 140℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
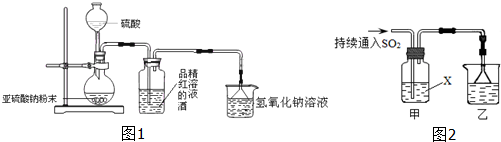
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ |
| C、①③④ | D、①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
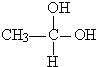 →CH3-CHO+H2O
→CH3-CHO+H2O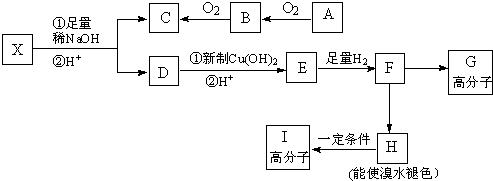
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com