
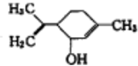
| A、能与氢氧化钠溶液发生中和反应 |
| B、能发生加成反应和取代反应 |
| C、不能使酸性高锰酸钾溶液褪色 |
D、与对丙基苯甲醇( )互为同分异构体 )互为同分异构体 |
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入KSCN溶液和盐酸,溶液变红色 | 原溶液一定含Fe3+ |
| B | 向某溶液中加入稀盐酸,产生使澄清石灰水变浑浊的无色无味气体 | 原溶液一定含CO32- |
| C | 向某溶液中加入稀盐酸无现象,再滴加BaCl2有白色沉淀 | 原溶液一定含SO42- |
| D | 向某溶液滴加稀NaOH溶液时,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 原溶液一定不含NH4+ |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 有两只密闭容器A和B,A能保持恒压,B能保持恒容.起始时向容积相等的A、B中分别通入体积比为2:1的等量的SO2和O2,使之发生反应:2SO2+O2?2SO3,并达到平衡.则(填>、=、<;左、右;增大、减小、不变).
有两只密闭容器A和B,A能保持恒压,B能保持恒容.起始时向容积相等的A、B中分别通入体积比为2:1的等量的SO2和O2,使之发生反应:2SO2+O2?2SO3,并达到平衡.则(填>、=、<;左、右;增大、减小、不变).查看答案和解析>>
科目:高中化学 来源: 题型:
 如图表示可逆反应A(g)+B(g)?nC(g)△H<0,在不同条件下反应混合物中C的质量分数C%和反应过程所需时间的关系曲线,有关叙述一定正确的是( )
如图表示可逆反应A(g)+B(g)?nC(g)△H<0,在不同条件下反应混合物中C的质量分数C%和反应过程所需时间的关系曲线,有关叙述一定正确的是( )| A、a表示有催化剂,而b无催化剂 |
| B、若其他条件相同,a比b的温度高 |
| C、若其他条件相同,a比b的压强大,n=l |
| D、反应由逆反应方向开始 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、a、b不连接时,只锌片上有气泡逸出,锌片逐渐溶解 |
| B、a和b用导线连接时,H+从铜片上获得锌失去的电子 |
| C、a和b是否用导线连接,装置中所涉及的化学反应都相同 |
| D、a和b是否用导线连接,装置中都是化学能转变为电能过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
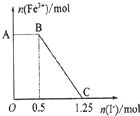 已知酸性高锰酸钾溶液可以将FeSO4氧化,MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O现将一定量酸性高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.则下列说法不正确的是( )
已知酸性高锰酸钾溶液可以将FeSO4氧化,MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O现将一定量酸性高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.则下列说法不正确的是( )| A、图中AB段主要是高锰酸钾和碘化钾溶液反应 |
| B、图中BC段发生的反应为2Fe3++2I-═2Fe2++I2 |
| C、根据OC段数据可知开始加入的高锰酸钾的物质的量为0.25 mol |
| D、根据OC段的数据可知开始加入的硫酸亚铁的物质的量为l mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
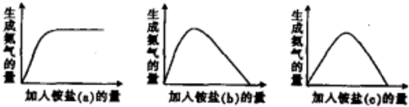
| A、a对应的铵盐是(NH4)2SO4 |
| B、b对应的铵盐是(NH4)2SO4和NH4HSO4 |
| C、c对应的铵盐是NH4HSO4 |
| D、当b和c铵盐的质量相同时,可得到相同量的氨气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com