
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取,纯净的A为无色粘稠液体,易溶于水.为研究A的组成与结构,进行实验如表所示:
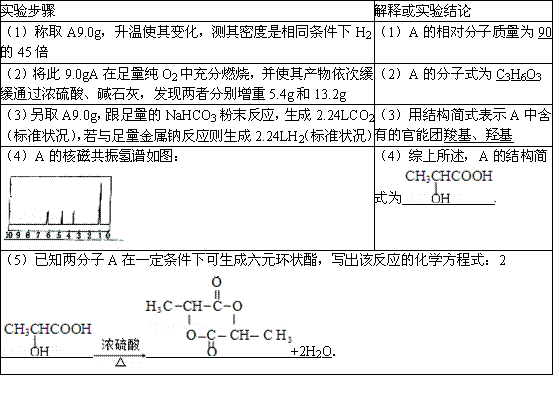
考点:有关有机物分子式确定的计算.
分析:(1)相同条件下,气体的相对分子质量之比等于密度之比;
(2)浓硫酸可以吸收水,碱石灰可以吸收二氧化碳,根据元素守恒来确定有机物的分子式;
(3)羧基可以和碳酸氢钠发生化学反应生成二氧化碳,﹣OH、﹣COOH和金属钠发生化学反应生成氢气,根据生成气体物质的量判断含有的官能团;
(4)核磁共振氢谱图中有几个峰值则含有几种类型的等效氢原子,峰面积之比等于氢原子的数目之比,结合A的分子式、含有的官能团确定A的结构简式;
(5)根据A的结构简式书写.
解答: 解:(1)有机物质的密度是相同条件下H2的45倍,所以有机物质的相对分子质量=45×2=90,
故答案为:90;
(2)9.0gA的物质的量=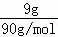 =0.1mol,浓硫酸增重5.4g,则生成水的质量是5.4g,生成n(H2O)=
=0.1mol,浓硫酸增重5.4g,则生成水的质量是5.4g,生成n(H2O)=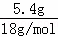 =0.3mol,所含有n(H)=0.6mol,碱石灰增重13.2g,生成m(CO2)是13.2g,n(CO2)=
=0.3mol,所含有n(H)=0.6mol,碱石灰增重13.2g,生成m(CO2)是13.2g,n(CO2)= =0.3mol,所以n(C)=0.3mol,n(A):n(C):n(H)=0.1mol:0.3mol:0.6mol=1:3:6,则有机物中碳个数是3,氢个数是6,根据相对分子质量是90,所以氧原子个数=
=0.3mol,所以n(C)=0.3mol,n(A):n(C):n(H)=0.1mol:0.3mol:0.6mol=1:3:6,则有机物中碳个数是3,氢个数是6,根据相对分子质量是90,所以氧原子个数=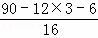 =3,即分子式为:C3H6O3,
=3,即分子式为:C3H6O3,
故答案为:C3H6O3;
(3)9.0gA的物质的量为0.1mol,A和碳酸氢钠反应说明A中含有羧基,生成2.24LCO2(标准状况),n(CO2)= =0.1mol,所以含有一个羧基;
=0.1mol,所以含有一个羧基;
醇羟基和羧基都可以和金属钠发生反应生成氢气,与足量金属钠反应则生成2.24LH2(标准状况),
n(H2)= =0.1mol,羧基或羟基与钠反应生成氢气时,羧基或羟基的物质的量与氢气的物质的量之比为2:1,A与钠反应时,A的物质的量与氢气的物质的量之比是1:1,则说明A中除了含有一个羧基外还含有一个羟基,
=0.1mol,羧基或羟基与钠反应生成氢气时,羧基或羟基的物质的量与氢气的物质的量之比为2:1,A与钠反应时,A的物质的量与氢气的物质的量之比是1:1,则说明A中除了含有一个羧基外还含有一个羟基,
故答案为:羧基、羟基;
(4)根据核磁共振氢谱图看出有机物中有4个峰值,则含4种类型的等效氢原子,且氢原子的个数比是3:1:1:1,所以结构简式为: ,
,
故答案为: ;
;
(5) 在一定条件下反应生成含六元环化合物的化学方程式为:2
在一定条件下反应生成含六元环化合物的化学方程式为:2

 +2H2O,
+2H2O,
故答案为:2

 +2H2O.
+2H2O.
点评:本题是一道关于有机物的结构和性质知识的综合推断题,考查学生对知识的整合能力,难度中等,注意根据A和碳酸氢钠、钠反应时生成气体体积判断含有的官能团.


科目:高中化学 来源: 题型:
⑴常温下0.1 mol·L-1的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是________;
A.c(H+) B.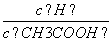 C.c(H+)·c(OH-) D.
C.c(H+)·c(OH-) D.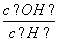
⑵体积为10 mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1 000 mL,稀释过程pH变化如图:则HX的电离平衡常数________(填“大于”、“等于”或“小于”)醋酸的平衡常数;理由是____________________________________________________,
(3)H+浓度相同等体积的两份溶液A(盐酸)和B(CH3COOH)分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是________(填写序号)。
①反应所需要的时间B>A ②开始反应时的速率A>B
③参加反应的锌的物质的量A=B ④反应过程的平均速率B>A
⑤A中有锌剩余 ⑥B中有锌剩余
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组利用废弃铝矿(含CuO、Al2O3及SiO2),模拟工业上提取铝的工艺,设计如下图所示的简单操作流程:

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:

回答下列问题:
(1)滤渣主要成分的化学式为______________________。
(2)灼烧Al(OH)3时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有___________(填仪器名称)。
(3)溶液Y中要加入稍过量原料A,原料A的化学式是_________。
(4)操作流程中③的离子方程式为_______________________。
(5)铝电池性能优越,Al—Ag2O电池可用作水下动力电源,其原理如图所示:

请写出该电池正极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:乙醇可被强氧化剂氧化为乙酸.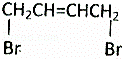 可经四步反应制取HOOCCH=CHCOOH.
可经四步反应制取HOOCCH=CHCOOH.
(1)第二步的反应类型是 :
(2)该制取过程中第二步的目的是: :
(3)写出第四步反应的化学方程式: :
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
A. 向漂白粉溶液中通入少量二氧化硫:Ca2++2ClO﹣+SO2+H2O═CaSO3↓+2HClO
B. 稀硝酸中加入过量铁粉:Fe+4H++NO﹣3═Fe3++NO↑+2H2O
C. 溴化亚铁溶液中通入足量氯气:2Fe2++2Br﹣+2Cl2═2Fe3++Br2+4Cl﹣
D. 苯酚钠溶液中通入少量二氧化碳: ﹣O﹣+CO2+H2O→
﹣O﹣+CO2+H2O→ ﹣OH+HCO3﹣
﹣OH+HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
Q、R、X、Y、Z五种元素的原子序数依次递增.已知:
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子排布为msnmpn;
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4.
请回答下列问题:
(1)Z2+的核外电子排布式是 .
(2)在[Z(NH3)4]2+离子中,Z2+的空轨道接受NH3分子提供的 形成配位键.
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 .
a.稳定性:甲>乙,沸点:甲>乙 b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小至大的顺序为 (用元素符号作答).
(5)Q的一种氢化物相对分子质量为26,其分子中σ键与π键的键数之比为 .
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于 (填晶体类型).
查看答案和解析>>
科目:高中化学 来源: 题型:
相对分子质量为a的某物质在室温下的溶解度为bg,此时测得饱和溶液的密度为c g·cm-3,则该饱和溶液的物质的量浓度是
A.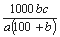 mol·L-1 B.
mol·L-1 B.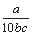 mol·L-1
mol·L-1
C.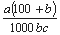 mol·L-1 D.
mol·L-1 D.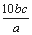 mol·L-1
mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com